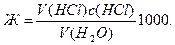приготовить 1 нормальный раствор соляной кислоты
Растворы кислот
Приблизительные растворы. В большинстве случаев в лаборатории приходится пользоваться соляной, серной и азотной кислотами. Кислоты имеются в продаже в виде концентрированных растворов, процентное содержание которых определяют по их плотности.
Кислоты, применяемые в лаборатории, бывают технические и чистые. Технические кислоты содержат примеси, а потому при аналитических работах не употребляются.
Концентрированная соляная кислота на воздухе дымит, поэтому работать с ней нужно в вытяжном шкафу. Наиболее концентрированная соляная кислота имеет плотность 1,2 г/см3 и содержит 39,11%’ хлористого водорода.
Разбавление кислоты проводят по расчету, описайному выше.
Пример. Нужно приготовить 1 л 5%-ного раствора соляной кислоты, пользуясь раствором ее с плотностью 1,19 г/см3. По справочнику узнаем, что 5%,-ный раствор нмеет плотность 1,024 г/см3; следовательно, 1 л ее будет весить 1,024*1000 = 1024 г. В этом количестве должно содержаться чистого хлористого водорода:
Кислота с плотностью 1,19 г/см3 содержит 37,23% HCl (находим также по справочнику). Чтобы узнать, сколько следует взять этой кислоты, составляют пропорцию:
или 137,5/1,19 = 115,5 кислоты с плотностью 1,19 г/см3, Отмерив 116 мл раствора кислоты, доводят объем его до 1 л.
Так же разбавляют серную кислоту. При разбавлении ее следует помнить, что нужно приливать кислотук воде
, а не наоборот. При разбавлении происходит сильное разогревание, и если приливать воду к кислоте, то возможно разбрызгивание ее, что опасно, так как серная кислота вызывает тяжелые ожоги. Если кислота попала на одежду или обувь, следует быстро обмыть облитое место большим количеством воды, а затем нейтрализовать кислоту углекислым натрием или раствором аммиака. При попадании на кожу рук или лица нужно сразу же обмыть это место большим количеством воды.
Особой осторожности требует обращение с олеумом, представляющим моногидрат серной кислоты, насыщенный серным ангидридом SO3. По содержанию последнего олеум бывает нескольких концентраций.
Следует помнить, что при небольшом охлаждении олеум закристаллизовывается и в жидком состоянии находится только при комнатной температуре. На воздухе он дымит с выделением SO3, который образует пары серной кислоты при взаимодействии с влагой воздуха.
Большие трудности вызывает переливание олеума из крупной тары в мелкую. Эту операцию следует проводить или под тягой, или на воздухе, но там, где образующаяся серная кислота и SO3 не могут оказать какого-либо вредного действия на людей и окружающие предметы.
Если олеум затвердел, его следует вначале нагреть, поместив тару с ним в теплое помещение. Когда олеум расплавится и превратится в маслянистую жидкость, его нужно вынести на воздух и там переливать в более мелкую посуду, пользуясь для этого способом передавлива-ния при помощи воздуха (сухого) или инертного газа (азота).
При смешивании с водой азотной кислоты также происходит разогревание (не такое, правда, сильное, как в случае серной кислоты), и поэтому меры предосторожности должны применяться и при работе с ней.
В лабораторной практике находят применение твердые органические кислоты. Обращение с ними много проще и удобнее, чем с жидкими. В этом случае следует заботиться лишь о том, чтобы кислоты не загрязнялись чем-либо посторонним. При необходимости твердые органические кислоты очищают перекристаллизацией (см, гл. 15 «Кристаллизация»),
Точные растворы. Точные растворы кислот готовят так же, как и приблизительные, с той только разницей, что вначале стремятся получить раствор несколько большей концентрации, чтобы после можно было его точно, по расчету, разбавить. Для точных растворов берут только химически чистые препараты.
Нужное количество концентрированных кислот обычно берут по объему, вычисленному на основании плотности.
Пример. Нужно приготовить 0,1 и. раствор H2SO4. Это значит, что в I л раствора должно содержаться:
Кислота с плотностью 1,84 г\смг содержит 95,6% H2SO4 н для приготовления 1 л 0,1 н. раствора нужно взять следующее количество (х) ее (в г):
Соответствующий объем кислоты составит:
Отмерив из бюретки точно 2,8 мл кислоты, разбавляют ее до 1 л в мерной колбе и затем титруют раствором щелочи п устанавливают нормальность полученного раствора. Если раствор получится более концентрированный), к нему добавляют из бюретки рассчитанное количество воды. Например, при титровании установлено, что 1 мл 6,1 н. раствора H2SO4 содержит не 0,0049 г H2SO4, а 0,0051 г. Для вычисления количества воды, которое необходимо для приготовления точно 0,1 н. раствора, составляем пропорцию:
Расчет показывает, что этот объем равен 1041 мл раствор нужно добавить 1041 — 1000 = 41 мл воды. Следует еще учесть то количество раствора, которое взято для титрования. Пусть взято 20 мл, что составляет 20/1000 = 0,02 от имеющегося объема. Следовательно, воды нужно добавить не 41 мл, а меньше: 41 — (41*0,02) = = 41 —0,8 = 40,2 мл.
Исправленный раствор следует снова проверить на содержание вещества, взятого для растворения. Точные растворы соляной кислоты готовят также ионообменным способом, исходя из точной рассчитанной навески хлористого натрия. Рассчитанную и отвешенную на аналитических весах навеску растворяют в дистиллированной или деминерализованной воде, полученный раствор пропускают через хроматографическую колонку, наполненную катионитом в Н-форме. Раствор, вытекающий из колонки, будет содержать эквивалентное количество HCl.
Как правило, точные (или титрованные) растворы следует сохранять в плотно закрытых колбах, В пробку сосуда обязательно нужно вставлять хлоркальциевую трубку, заполненную в случае раствора щелочи натронной известью или аскаритом, а в случае кислоты — хлористым кальцием или просто ватой.
Для проверки нормальности кислот часто применяют прокаленный углекислый натрий Na2COs. Однако он обладает гигроскопичностью и поэтому не полностью удовлетворяет требованиям аналитиков. Значительно удобнее пользоваться для этих целей кислым углекислым калием KHCO3, высушенным в эксикаторе над CaCl2.
При титровании полезно пользоваться «свидетелем», для приготовления которого в дистиллированную или деминерализованную воду добавляют одну каплю кислоты (если титруют щелочь) или щелочи (если титруют кислоту) и столько капель индикаторного раствора, сколько добавлено в титруемый раствор.
Приготовление эмпирических, по определяемому веществу, и стандартных растворов, кислот проводят по расчету с применением формул, приведенных для этих и описанных выше случаев.
Приготовление 250 мл приблизительно 0,1 н. раствора HCl.
Рассчитывают необходимое количество соляной кислоты. Для этого, измеряют удельный вес кислоты, определяют ее процентное содержание в растворе и рассчитывают необходимое количество (мл) HCl.
в 100 г раствора содержится 38,8 г HCl,
в Х г раствора содержится 3,646 г HCl,
Х = (100 · 3,646)/38,3 = 9,52 г.
При пересчете найденного весового количества кислоты на объем (V) получаем:
Нам нужно приготовить 250 мл раствора, поэтому количество кислоты, необходимое для приготовления раствора будет в 4 раза меньше, т.е 2,0 мл.
Отмерив вычисленный объем пипеткой, переносят его в мерную колбу и доводят до метки дистиллированной водой. Полученный раствор тщательно перемешивают (табл.1).
Удельный вес соляной кислоты различной концентрации при 20°С
| Удельный вес | HCl (%) | Удельный вес | HCl (%) |
| 1,160 | 32,1 | 1,180 | 36,2 |
| 1,165 | 33,2 | 1,185 | 37,3 |
| 1,170 | 34,2 | 1,190 | 38,3 |
| 1,175 | 35,2 | 1,195 | 39,37 |
Стандартизация раствора соляной кислоты по тетраборату натрия. Титрование ведется с метиловым оранжевым, приливая кислоту из бюретки к раствору тетрабората натрия.
Тщательно вымытую бюретку ополосните небольшими порциями кислоты для удаления остатков воды. Пользуясь воронкой, наполните бюретку кислотой так, чтобы мениск ее был несколько выше нулевого деления. Заполните раствором оттянутую трубку, вытеснив из нее пузырьки воздуха. Затем уберите воронку, так как с нее может капать раствор, и, выпуская лишнюю кислоту, установите нижний край мениска на нулевом делении. В таком состоянии бюретка готова к работе.
Чистую пипетку вместимостью 10 мл ополосните раствором тетрабората натрия и отмерьте 10,00 мл его в коническую колбу для титрования. Не выдувайте из пипетки последнюю каплю жидкости, только прикоснитесь концом ее к стенке колбы. Прилейте к отмеренному раствору тетрабората натрия одну каплю метилового оранжевого.
На основание штатива положите лист белой бумаги, подставьте колбу с исходным раствором тетрабората натрия под бюретку и приступайте к титрованию. Первое титрование считается ориентировочным. Но затем добейтесь того, чтобы желтая окраска метилового оранжевого переходила в бледно-розовую от одной избыточной капли кислоты.
Титрование повторяйте до получения сходящихся результатов, т.е. пока отсчеты будут отличаться друг от друга не более чем на 0,1 мл. Все результаты титрования записывайте в журнал. Из 2-3 результатов возьмите среднее арифметическое и вычислите нормальную концентрацию раствора кислоты.
Средний расход рабочего раствора равен
Так как VHCl · N1 = V2 · N2, где VHCl и N1 – объем и нормальность HCl, а V2 и N2 – объем и нормальность тетрабората натрия, то вычисляем по данной формуле N1.
2.2. Определение нормальности раствора щелочи с помощью раствора соляной кислоты
Нормальность раствора щелочи устанавливается по раствору соляной кислоты точной концентрации, пользуясь правилом N1V1 = N2V2, откуда
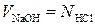
Для определения нормальности раствора щелочи устанавливаем объемное соотношение между вступающими в реакцию растворами кислоты и щелочи.
2.3. Определение карбонатной жесткости воды
С помощью стандартизированного раствора хлороводородной кислоты определяют не только содержание щелочей, но и некоторых солей. Большое практическое значение имеет определение карбонатной жесткости воды.
Известно, что жесткость обусловлена присутствием в воде растворимых солей кальция и магния.
Карбонатная жесткость зависит от содержания в воде растворимых солей кальция и магния. Она почти полностью устраняется кипячением, при котором гидрокарбонаты разлагаются
Поэтому карбонатную жесткость называют также устранимой или временной.
Некарбонатная жесткость вызывается присутствием в воде сульфатов (а также хлоридов) кальция или магния.
Карбонатную жесткость определяют титрованием определенного объема воды раствором НСl с метиловым оранжевым. Химизм процесса выражается уравнениями
Ход определения.В коническую колбу отмерьте пипеткой 100,0 мл анализируемой воды. Прибавьте 2-3 капли метилового оранжевого и титруйте раствором НСl до перехода желтой окраски индикатора в бледно-розовую. Повторите титрование 2-3 раза и из сходящихся отсчетов возьмите среднее. Удобно выполнять титрование со «свидетелем».
Чтобы вычислить карбонатную жесткость (по ГОСТу) в моль на 1 л воды, находят нормальную концентрацию раствора солей и умножают ее на 1000
Допустим, что на титрование 100,0 мл воды пошло в среднем 12,25 мл 0,1016 н. раствора кислоты. Тогда
Ж = (12,25 ∙ 0,1016/100)1000 = 12,45.
2.4. Определение гидроксида и карбоната натрия при совместном присутствии в растворе.
Гидроксид натрия (как и другие щелочи) поглощает из воздуха оксид углерода (IV) и частично превращается в карбонат натрия
Поэтому часто определяют содержание NaOH и Na2CO3 при совместном присутствии их в растворе.
Титрование такого раствора кислотой можно рассматривать как процесс, протекающий в две стадии
Первая стадия завершается при рН 8,31, когда изменяет окраску фенолфталеин, а вторая – при рН 3,84, т.е. в области перехода метилового оранжевого.
Из уравнения реакции видно, что с фенолфталеином оттитровывается весь NaOH и половина карбоната натрия. Оставшуюся половину карбоната натрия дотитровывают с метиловым оранжевым.
Точность этого метода, основанного на определении двух точек эквивалентности, не превышает 1%. Объясняется это тем, что в процессе титрования раствор может поглощать оксид углерода (IV) из воздуха и часть NaOH будет превращаться в карбонат натрия. Чтобы свести до минимума это нежелательное явление, соблюдают следующие правила. Раствор щелочи разбавляют водой, свободной от оксида углерода (IV), т.е. прокипяченной и охлажденной в сосуде, имеющем поглотительную трубку с известью. Быстро переносят пипеткой раствор в коническую колбу и тотчас титруют его кислотой, избегая сильного перемешивания (усиливающего поглощение CO2 из воздуха).
Для титрования приходится брать довольно много (4-5 капель) фенолфталеина, так как небольшие количества его могут обесцвечиваться еще до точки эквивалентности (под действием CO2 воздуха). Заканчивая титрование раствора с фенолфталеином, кислоту прибавляют медленно, чтобы вместо гидрокарбоната натрия не получилась угольная кислота.
Ход определенияВ мерную колбу вместимостью 100 мл возьмите немного анализируемого раствора, разбавьте его до метки свежепрокипяченной дистиллированной водой и тщательно перемешайте. Перенесите пипеткой 10,0 мл раствора в коническую колбу и прибавьте 4-5 капель фенолфталеина, который окрасит жидкость в малиновый цвет. Титруйте его раствором НСl до обесцвечивания, которое должно произойти от одной избыточной капли кислоты. Запишите отчет. Затраченный объем кислоты соответствует всему определяемому гидроксиду натрия и половине карбоната натрия.
После этого прибавьте к титруемому раствору 1-2 капли метилового оранжевого, в результате чего содержимое колбы окрасится в желтый цвет. Не доливая кислоту в бюретку, продолжайте титровать раствор до перехода желтой окраски в бледно-розовую. Запишите второй отсчет (т.е. расход кислоты на титрование половины карбоната натрия).
Точное титрование с фенолфталеином и метиловым оранжевым повторите 2-3 раза и из сходящихся отсчетов возьмите средние данные.
Вычислите массы NaOH и Na2CO3 в анализируемом растворе.
Допустим, что после титрования раствора с фенолфталеином отсчет объема кислоты оказался равен 11,60 мл, а после титрования с метиловым оранжевым – 12,30 мл.
Следовательно, на титрование половины Na2CO3 израсходовано 12,30−11,60 = 0,70 мл, а на титрование всего карбоната натрия 0,70 
Например, нормальная концентрация раствора по карбонату натрия равна
с(Na2CO3)10,00 = 0,1016 ∙ 1,40, с(Na2CO3) = 0,1016 · 1,40/10,00 = 0,01422, где 0,01016 – нормальная концентрация раствора кислоты.
Остается вычислить массу карбоната натрия, содержащуюся в 0,1 л анализируемого раствора
Аналогичным образом вычисляют нормальную концентрацию раствора по гидроксиду натрия и его массу в 100 мл раствора.
Раздел 3. Перманганатометрическое титрование
3.1. Сущность перманганатометрического титрования.
Перманганатометрическое титрование – метод анализа, в котором титрантом служит раствор перманганата калия. В процессе титрования анализируемого раствора малиново-фиолетовая окраска раствора перманганата обесцвечивается. Однако после достижения точки эквивалентности первая же избыточная капля раствора перманганата окрашивает тируемую жидкость в розовый цвет. Индикатором в данном случае является перманганат калия. Поэтому при перманганатометрических определениях посторонние индикаторы не добавляют.
Используют кривые окислительно-восстановительного титрования, в частности перманганатометрического титрования. Но если кривые кислотно-основного титрования показывают зависимость степени оттитрованности от рН раствора, то кривые перманганатометрического титрования выражают зависимость потенциала окислительно-восстановительной системы от степени оттитрованности, вблизи точки эквивалентности происходит резкий скачок редокс-потенциала.
При титровании в щелочной или нейтральной среде Mn(VII) восстанавливается до Mn(IV), например:
Образующийся MnO(OH)2 представляет собой бурый осадок, присутствие которого в растворе затрудняет определение точки эквивалентности. Кроме того, окислительная активность перманганата калия в кислой среде гораздо выше, чем в щелочной. По этим соображениям титрование перманганатом калия чаще всего проводят в кислых растворах.
Перманганатометрию используют для количественного определения не только восстановителей, но и окислителей. Восстановители, за редким исключением, определяют прямым титрованием раствором перманганата. Определяя окислители, пользуются приемом обратного титрования, т.е. к анализируемому раствору окислителя приливают заведомый избыток вспомогательного раствора восстановителя с известной концентрацией, затем остаток восстановителя оттитровывают раствором перманганата калия и делают расчет.
3.2. Приготовление стандартизированного раствора перманганата калия.
Титрованный раствор перманганата калия нельзя приготовить растворением точной навески: продаваемый перманганат калия содержит ряд примесей. Кроме того концентрация перманганата калия, переведенного в раствор, заметно понижается, так как он расходуется на взаимодействие с аммиаком, органическими веществами, которые попадают в воду с пылью. Поэтому нормальную концентрацию раствора перманганата калия устанавливают обычно лишь через 5-7 дней после его приготовления. Исходными веществами для стандартизации его служат свежеперекристаллизованная щавелевая кислота H2C2O4∙2H2O или ее соли Na2C2O4 и (NH4)2C2O4∙H2O.
Приготовление стандартного раствора щавелевой кислоты. Перманганат калия взаимодействует с щавелевой кислотой в сернокислой среде по уравнению
Аналогично взаимодействует он и с оксалатами
Очевидно, молярная масса эквивалента щавелевой кислоты H2C2O4∙2H2O, которой мы воспользуемся как стандартным веществом, равна ½ молярной массы, т.е. 126,07/2 = 63,04 г/моль. Для приготовления 100 мл 0,05 н. раствора нужно взять: 63,04 ∙ 0,05 ∙ 0,1 = 0,3152 г щавелевой кислоты.
Возьмите навеску H2C2O4∙2H2O на аналитических весах, растворите ее в мерной колбе вместимостью 100 мл, доведите объем раствора водой до метки и тщательно перемешайте. Вычислите титр и нормальную концентрацию исходного раствора щавелевой кислоты. Допустим, что навеска щавелевой кислоты составила 0, 2988 г, тогда
Т = 0,2988/100 = 0,002988 г/мл,
а нормальная концентрация
с = 0,002988 ∙ 1000/63,04 = 0,04741.
Приготовление 250 мл приблизительно 0,05 н. раствора перманганата калия. Нормальную концентрацию раствора перманганата устанавливают по реакции, протекающей в кислой среде. В этом случае молярная масса эквивалента KMnO4 равна158,03/5 = 31,61 г/моль. Теоретически для приготовления 0,25 л 0,05 н. раствора следовало бы взять: 31,61 ∙ 0,05 ∙ 0,25 = 0,3951 г KMnO4. Но, учитывая, что продаваемый препарат не совсем чист и, кроме того, часть перманганата расходуется на окисление присутствующих в воде восстановителей, возьмите на весах 0,4 г KMnO4. Навеску растворите в 250 мл воды следующим образом: приливайте в стакан с навеской небольшие порции горячей воды, время от времени сливая жидкость с кристаллов в специально приготовленную мерную колбу. Растворение ускоряйте путем непрерывного перемешивания. Когда вся навеска перейдет в раствор, прилейте к нему оставшуюся воду, тщательно перемешайте, закройте пробкой и оставьте стоять в темном месте. При хранении раствора на свету происходит разложение перманганата калия
Тот же осадок MnO(OH)2 выделяется в результате взаимодействия перманганата с восстановителями.
Через 5-7 дней раствор, титр которого станет постоянным, осторожно слейте с осадка в другую склянку. Он нуждается еще в установке нормальной концентрации по исходному веществу.
Стандартизация раствора перманганата калия по щавелевой кислоте. Хорошо вымытую бюретку промойте раствором перманганата калия и подготовьте к титрованию.
Ополосните пипетку раствором щавелевой кислоты и перенесите 10,00 мл его в коническую колбу. Прибавьте 8-10 мл 2 н. серной кислоты, нагрейте до 70-80 ºС (не допуская кипения, при котором щавелевая кислота разлагается) и горячий раствор титруйте перманганатом калия.
Раствор перманганата калия приливайте медленно, по каплям, при непрерывном перемешивании. Каждую следующую каплю добавляйте лишь после того, как обесцветилась предыдущая. Первоначально обесцвечивание перманганата будет происходить медленно, но затем по мере образования сульфата марганца, играющего роль катализатора, оно ускорится. Титрование прекратите, когда избыточная капля перманганата сообщит раствору бледно-розовую окраску, не исчезающую в течение 1-2 мин. Объемы раствора перманганата калия отсчитывайте по верхнему краю мениска, так как нижний плохо виден. Повторите титрование 2-3 раза, из сходящихся отсчетов возьмите среднее значение и вычислите нормальную концентрацию раствора перманганата калия.
Например, если на титрование 10,00 мл 0,04741 н. раствора щавелевой кислоты пошло в среднем 9,15 мл раствора перманганата калия, нормальная концентрация его
с(KMnO4) = 0,04741 ∙ 10,00/9,15 = 0,05181.
Приготовить 1 нормальный раствор соляной кислоты
В анализах методом нейтрализации применяют 0,1 н. и 0,5 н. точные растворы серной и соляной кислот, а в других методах анализа, например в окислительно-восстановительном, часто используют 2 н. приблизительные растворы этих кислот.
Для быстрого приготовления точных растворов удобно пользоваться фиксаналами, представляющими собой навески (0,1 г-экв или 0,01 г-экв) химически чистых веществ, взвешенные с точностью до четырех-пяти значащих цифр, находящиеся в запаянных стеклянных ампулах. При приготовлении 1 л. раствора из фиксанала получают 0,1 н. или 0,01 н. растворы. Небольшие количества растворов соляной и серной кислот 0,1 н. концентрации можно готовить из фиксаналов. Стандартные растворы, приготовленные из фиксаналов, обычно служат для установления или проверки концентрации других растворов. Фиксаналы кислот можно хранить долгое время.
Для приготовления точного раствора из фиксанала ампулу обмывают теплой водой, смывая с нее надпись или этикетку, и хорошо обтирают. Если надпись сделана краской, то ее удаляют тряпочкой, смоченной спиртом. В мерную колбу емкостью 1 л. вставляют стеклянную воронку, а в нее — стеклянный боек, острый конец которого должен быть направлен вверх. После этого ампулу с фиксаналом слегка ударяют тонким дном об острие бойка или дают ей свободно падать, чтобы дно разбилось при ударе об острие. Затем стеклянным штырем с заостренным концом разбивают тонкую стенку углубления в верхней части ампулы и дают содержащейся в ампуле жидкости вытечь. Потом ампулу, находящуюся в воронке, тщательно промывают дистиллированной водой из промывалки, после чего удаляют из воронки, промывают воронку и удаляют ее из колбы, а раствор в колбе доливают до метки дистиллированной водой, закрывают пробкой и перемешивают.
При приготовлении растворов из сухих фиксаналов (например, из фиксанала щавелевой кислоты) берут сухую воронку, чтобы содержимое ампулы можно было при легком встряхивании пересыпать в колбу. После того как вещество перенесут в колбу, промывают ампулу и воронку, растворяют вещество в воде, находящейся в колбе, и доводят объем раствора дистиллированной водой до метки.
Большие количества 0,1 н. и 0,5 н. растворов соляной и серной кислот, а также приблизительные растворы этих кислот (2 н. и др.) готовят из концентрированных химически чистых кислот. Вначале ареометром или денсиметром определяют плотность концентрированной кислоты.
По плотности в справочных таблицах находят концентрацию кислоты (содержание хлористого водорода в соляной кислоте или моногидрата в серной), выраженную в граммах на 1 л. По формулам рассчитывают объем концентрированной кислоты, необходимый для приготовления заданного объема кислоты соответствующей концентрации. Расчет проводят с точностью до двух-трех значащих цифр. Количество воды для приготовления раствора определяют по разности объемов раствора и концентрированной кислоты.
Раствор соляной кислоты готовят путем приливания в сосуд для приготовления раствора половины требуемого количества дистиллированной воды, а затем концентрированной кислоты; после перемешивания раствор доливают до полного объема оставшимся количеством воды. Частью второй порции воды ополаскивают мензурку, которой отмеривали кислоту.
Раствор серной кислоты готовят путем медленного приливания концентрированной кислоты при постоянном перемешивании (чтобы не допустить разогревания) к воде, налитой в сосуд из термостойкого стекла. При этом небольшое количество воды оставляют для ополаскивания мензурки, которой отмеривали кислоту, приливая этот остаток в раствор после его охлаждения.
Иногда для химического анализа применяют растворы твердых кислот (щавелевой, винной и др.). Эти растворы готовят растворением в дистиллированной воде навески химически чистой кислоты.
Массу навески кислоты вычисляют по формуле. Объем воды для растворения берут приблизительно равным объему раствора (если растворение ведется не в мерной колбе). Для растворения этих кислот применяют воду, не содержащую углекислого газа.
Пример 1. Рассчитать количество концентрированной соляной кислоты плотности 1,14 г/см 3 и количество воды, необходимое для приготовления 10 л 0,1 н. раствора.
В таблице по плотности находим содержание хлористого водорода HCl в концентрированной кислоте: Гк = 315 г/л.
Рассчитываем объем концентрированного раствора соляной кислоты:
Vк = 36,5N•V / Тк = 36,5•0,1•10000 / 315 = 315 мл.
Количество воды, необходимое для приготовления раствора:
Пример 2. Рассчитать количество щавелевой кислоты, необходимое для приготовления 2 л 0,1 н. раствора.
Масса навески щавелевой кислоты H2C2O4•2H2O:
63,03N•V / 1000 = 63,03•0,1•3000 / 1000 = 12,6 г.
Установление концентрации рабочих растворов кислот можно проводить по карбонату натрия, буре, точному раствору щелочи (титрованному или приготовленному из фиксанала). При установлении концентрации растворов соляной или серной кислот по карбонату натрия или по буре пользуются методом титрования навесок или (реже) методом пипетирования. При методе титрования навесок используют бюретки емкостью 50 или 25 мл.
При установлении концентрации кислот большое значение имеет выбор индикатора. Титрование выполняют в присутствии такого индикатора, у которого переход окраски происходит в интервале pH, соответствующем точке эквивалентности для химической реакции, протекающей при титровании. При взаимодействии сильной кислоты с сильным основанием в качестве индикаторов можно использовать метиловый оранжевый, метиловый красный, фенолфталеин и другие, у которых переход окраски происходит при pH = 4?10.
При взаимодействии сильной кислоты со слабым основанием или с солями слабых кислот и сильных оснований в качестве индикаторов используют такие, у которых переход окраски происходит в кислой среде, например метиловый оранжевый. При взаимодействии слабых кислот с сильными щелочами применяют индикаторы, у которых переход окраски происходит в щелочной среде, например фенолфталеин. Концентрацию раствора нельзя определить титрованием, если при титровании взаимодействует слабая кислота со слабым основанием.
При установлении концентрации соляной или серной кислот по карбонату натрия на аналитических весах в отдельных бюксах берут три-четыре навески безводного химически чистого карбоната натрия с точностью до 0,0002 г. Для установления концентрации 0,1 н. раствора путем титрования из бюретки емкостью 50 мл масса навески должна быть около 0,15 г. Сушкой в сушильном шкафу при 150°С навески доводят до постоянной массы, а затем переносят в конические колбы емкостью 200—250 мл и растворяют в 25 мл дистиллированной воды. Бюксы с остатками карбоната взвешивают и по разности масс определяют точную массу каждой навески.
Титрование раствора карбоната натрия кислотой ведут в присутствии 1—2 капель 0,1%-ного раствора метилового оранжевого (титрование заканчивается в кислой среде) до изменения желтой окраски раствора в оранжево-желтую. При титровании полезно пользоваться раствором — «свидетелем», для приготовления которого в дистиллированную воду, налитую в такую же колбу, как и колба, в которой производится титрование, добавляют одну каплю кислоты из бюретки и столько капель индикатора, сколько его добавляют в титруемый раствор.
Объем дистиллированной воды для приготовления раствора — «свидетеля» должен быть примерно равен объему раствора в колбе в конце титрования.
Нормальную концентрацию кислоты рассчитывают по результатам титрования:
где mн — масса навески соды, г;
V — объем раствора кислоты (мл), израсходованный на титрование.
Из нескольких опытов берут среднюю сходящуюся величину концентрации.
Пример 3. Рассчитать массу навески карбоната натрия для установления концентрации 0,1 н. раствора серной кислоты, если для титрования используют бюретку емкостью 25 мл.
Предполагаем израсходовать на титрование около 20 мл кислоты.
Масса навески соды:
52,99 • 0,1 • 20 / 1000 = 0,1 г.
Пример 4. Навеска карбоната натрия в 0,1482 г оттитрована 28,20 мл раствора соляной кислоты. Определить концентрацию кислоты.
Нормальная концентрация соляной кислоты:
1000 • 0,1482 / 52,99 • 28,2 = 0,1012 н.
При установлении концентрации раствора кислоты по карбонату натрия методом пипетирования навеску химически чистого карбоната натрия, предварительно доведенную высушиванием в сушильном шкафу до постоянной массы и взвешенную с точностью до 0,0002 г, растворяют в дистиллированной воде в откалиброванной мерной колбе емкостью 100 мл.
Величина навески при установлении концентрации 0,1 н. раствора кислоты должна быть около 0,5 г (чтобы при растворении получить примерно 0,1 н. раствор). На титрование берут пипеткой 10—25 мл раствора карбоната натрия (в зависимости от емкости бюретки) и 1—2 капли 0,1%-ного раствора метилового оранжевого.
Метод пипетирования часто применяют при установлении концентрации растворов с помощью полумикробюреток емкостью 10 мл с ценой деления 0,02 мл.
Нормальную концентрацию раствора кислоты при ее установлении методом пипетирования по карбонату натрия вычисляют по формуле:
где mн — масса навески карбоната натрия, г;
V1 — объем раствора карбоната, взятый на титрование, мл;
Vк — объем мерной колбы, в которой производилось растворение навески карбоната;
V2 — объем раствора кислоты, израсходованный на титрование.
Пример 5. Определить концентрацию раствора серной кислоты, если для ее установления 0,5122 г карбоната натрия было растворено в мерной колбе емкостью 100,00 мл и на титрование 15,00 мл раствора карбоната израсходовано 14,70 мл раствора кислоты (при использовании бюретки емкостью 25 мл).
Нормальная концентрация раствора серной кислоты:
1000 • 0,5122 • 15 / 52,99 • 100 • 14,7 = 0,09860 н.
При установлении концентрации серной или соляной кислот по тетраборату натрия (буре) обычно используют метод титрования навесок. Кристаллогидрат буры Na2B4O7•10H2O должен быть химически чистым и перед установлением по нему концентрации кислоты его подвергают перекристаллизации. Для перекристаллизации 50 г буры растворяют в 275 мл воды при 50—60°C; раствор фильтруют и охлаждают до 25—30°C. Энергично помешивая раствор, вызывают кристаллизацию. Кристаллы отфильтровывают на воронке Бюхнера, растворяют снова и перекристаллизовывают. После фильтрования кристаллы сушат между листами фильтровальной бумаги при температуре воздуха 20°C и относительной влажности воздуха 70%; сушку проводят на воздухе или в эксикаторе над насыщенным раствором хлорида натрия. Высушенные кристаллы не должны прилипать к стеклянной палочке.
Для титрования отбирают в бюкс поочередно 3—4 навески буры с точностью до 0,0002 г и переносят их в конические колбы для титрования, растворяя каждую навеску в 40—50 мл теплой воды при энергичном взбалтывании. После перенесения каждой навески из бюкса в колбу бюкс взвешивают. По разности масс при взвешивании определяют величину каждой навески. Величина отдельной навески буры для установления концентрации 0,1 н. раствора кислоты при применении бюретки емкостью 50 мл должна быть около 0,5 г.
Титрование растворов буры кислотой ведут в присутствии 1—2 капель 0,1%-ного раствора метилового красного до изменения желтой окраски раствора в оранжево-красную или в присутствии раствора смешанного индикатора, состоящего из метилового красного и метиленового синего.
Нормальную концентрацию раствора кислоты рассчитывают по формуле:
где mн — масса навески буры, г;
V — объем раствора кислоты, израсходованный на титрование, мл.
Пример 6. Рассчитать навеску буры для установления концентрации 0,1 н. раствора соляной кислоты методом титрования навесок при применении бюретки емкостью 25 мл.
На титрование предполагается израсходовать 15 мл раствора кислоты.
Масса навески буры:
190,69 • 0,1 • 15 / 1000 = 0,3 г.
Пример 7. Найти концентрацию раствора соляной кислоты, если для титрования навески буры в 0,4952 г израсходовано 24,38 мл соляной кислоты.
1000 • 0,4952 / 190,624,38 = 0,1068
Установление концентрации кислоты по раствору едкого натра или едкого кали проводят путем титрования раствором кислоты раствора щелочи в присутствии 1—2 капель 0,1%-ного раствора метилового оранжевого. Однако этот метод установления концентрации кислоты менее точный, чем приведенный выше. Его обычно используют при контрольных проверках концентрации кислот. В качестве исходного раствора часто пользуются раствором щелочи, приготовленным из фиксанала.
Нормальную концентрацию раствора кислоты N2 рассчитывают по формуле:
где N1 — нормальная концентрация раствора щелочи;
V1 — объем раствора щелочи, взятый для титрования;
V2 — объем раствора кислоты, израсходованный на титрование (средняя величина сходящихся результатов титрования).
Пример 8. Определить концентрацию раствора серной кислоты, если на титрование 25,00 мл 0,1000 н. раствора едкого натра израсходовано 25,43 мл раствора серной кислоты.