Стимулятор диафрагмального нерва что это такое
Пациентам
Система стимуляции диафрагмального нерва представляет собой имплантируемый стимулятор, обеспечивающий поддержку пациентов с хронической вентиляционной недостаточностью и остаточной функцией диафрагмы, легких и диафрагмальных нервов. Повторные сигналы, посылаемые к диафрагмальным нервам, вызывают ровные и ритмичные сокращения диафрагмы, которые приводят ко вдоху воздуха в легкие.
Стимулятор состоит из электродов, прикрепляемых к диафрагмальным нервам, радиоприемников, помещенных в подкожные карманы, и внешнего блока Mark IV с передатчиком и антенной, который питает систему от батарей мощностью 9 вольт.
Внешний передатчик с помощью антенны передает на имплантируемый приемник радиосигнал, посылая к нему информацию о стимуляции. Приемник преобразует радиоволны в стимулирующие импульсы, которые доставляются к диафрагмальным нервам через электроды. Мышца диафрагмы сокращается, и происходит фаза вдоха. Затем передатчик прекращает производить сигналы, что позволяет диафрагме расслабляться (фаза выдоха). Повторение серии таких импульсов воспроизводит нормальное дыхание.
Перечень основных показаний включает в себя, но не ограничен следующими состояниями:
Преимущества стимулятора диафрагмы:
Стимулятор диафрагмы обеспечивает физиологическую дыхательную функцию гораздо лучше по сравнению с механической вентиляцией, поскольку вдыхаемый воздух попадает в легкие под действием мышц, естественным образом, а не за счет внешнего механического давления:
Многолетний опыт исследований в области разработки стимуляторов дыхания и годы их последующего применения показали, что их использование:
ОБЗОР СИСТЕМЫ
Передатчик Mark IV

В марте 1998 г. компания Avery Biomedical Devices получила разрешение Управления качества по контролю пищевых продуктов и лекарственных средства США (Food and Drug Agency, FDA) на использование передатчика Mark IV взрослыми пациентами и детьми, потерявшими неврологический контроль над дыханием. В 1994 г. передатчик Mark IV получил Европейский сертификат качества (CE Mark) в соответствии с действующей Европейской Директивой по имплантируемым медицинским устройствам.
Антенны 902A / 902AL
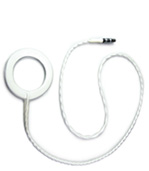
Антенна требует периодической замены в силу естественного износа в процессе использования (например, провод перекручивается или вырван из разъема/соединителя и т.д.), рекомендованный период — каждые шесть месяцев. Антенны не содержат латекс, при их производстве также не используются продукты из латекса. Инструкции по использованию антенн и уходу за ними доступны здесь.
Имплантируемые компоненты: приемник и электроды
Имплантируемые приемники — это небольшие устройства круглой формы, которые содержат в себе электронную схему, вставленную в эпоксидную смолу и покрытую силиконом. Каждый приемник преобразует энергию сигнала от антенн в четкие стимулирующие импульсы и передает их на электроды, прикрепленные к диафрагмальным нервам.
Имплантируемые электроды состоят из очень гибких волокон из нержавеющей стали, изолированных силиконом, с платиновым контактом для подсоединения к нерву на одном конце и соединителем для связи с принимающим устройством – на другом. Каждый электрод принимает стимулирующий импульс от приемника и передает его диафрагмальному нерву, вызывая тем самым сокращение мышц диафрагмы.
Транстелефонный монитор
Устройство для транстелефонного мониторинга (ТТМ) обеспечивает передачу количественных данных для обычного и диагностического контроля внешнего и имплантируемого оборудования системы, а также данные о физиологическом ответе пациента. Используя обычный телефон, можно послать сигнал производителю в любое время суток из любой точки мира. Переданный сигнал регистрируется на устройстве, подобном автоответчику, и анализ записи может быть сделан в течение одного рабочего дня. Каждый сигнал TTM анализируется, а результаты посылаются личному врачу пациента, чтобы помочь с медицинским диагнозом и лечением. Инструкция по отправке отчета находятся в Руководстве по использованию, прилагаемом к каждой системе стимуляции диафрагмального нерва. С данным документом можно также ознакомиться в разделе ВРАЧАМ.
Проведена первая в России операция по вживлению ребёнку стимулятора дыхания
На глазах у мамы Камиллу в 6 лет сбила машина. Она получила настолько тяжелые травмы головного и спинного мозга, что врачи не давали никаких шансов на то, что девочка очнется. Даже советовали отключить ее от систем жизнеобеспечения.
Почти 6 лет Камилла находилась в коме, ни на что не реагировала. Все это время мама девочки была рядом, делала массаж, читала книжки и просто разговаривала. В результате малышка очнулась, сегодня она узнает близких и даже улыбается. Для дальнейшей реабилитации необходимо Камиллу отключить от аппарата искусственной вентиляции легких, но самостоятельно она дышать не может.
Благодаря уникальной технологии шанс жить и развиваться нормально получит сегодня Камилла, а потом и тысячи детей по всей стране. В Научно-практическом центре медицинской помощи детям сегодня специалисты из России и США совместно выполнили операцию по имплантации стимулятора диафрагмального нерва.
Устройство имплантируют симметрично с двух сторон через небольшие разрезы. Основная часть стимулятора крепится к диафрагмальному нерву. Электроды, принимающие сигнал, находятся в области ключицы. Вдох происходит благодаря сокращению диафрагмы, самой большой дыхательной мышцы. Стимул поступает из этого устройства, пациент его носит всегда с собой. Параметры выставляют индивидуально и все время корректируют, ведь, по сути, ребенка учат заново дышать.
Разговаривать Илюша пока еще не может, потому что большую часть жизни за него дышал аппарат. Мальчик родился с редкой болезнью — синдромом Ундины. Это неофициальное название патологии, при которой остановка дыхания может произойти ночью во время сна. Два года назад, благодаря помощи зрителей Первого канала и Русфонда, в США мальчику имплантировали стимулятор дыхания. Многие родители уверены, что такое лечение можно получить только в зарубежных клиниках. До этого дня все так и было. Но теперь российские медики говорят, что готовы помочь абсолютно всем здесь, дома.
Стимулятор диафрагмального нерва что это такое
Государственное бюджетное учреждение здравоохранения города Москвы
«Научно-практический центр специализированной медицинской помощи детям имени В.Ф. Войно-Ясенецкого
Департамента здравоохранения города Москвы»
По рабочим дням с 8.30 до 16.30
Платные услуги: консультации, госпитализация, иные вопросы
По рабочим дням с 8.30 до 16.30
Приёмное отделение стационара
По рабочим дням с 8.30 до 16.30
Запись на прием/исследования по единому справочному тел.: 122, а также через ЕМИАС, инфоматы в холле, лично в регистратуре, www.pgu.ru и mos.ru
+7 (495) 735-09-57
(Канцелярия, ул. Авиаторов, д. 38);
+7 (499) 638-35-00 (Регистратура КДЦ)
+7 (499) 730-98-74
Справочный телефон по вопросам плановой госпитализации
 | +7 (495) 934-17-53, +7 (495) 439-27-10, +7 (495) 539-30-00 |
 | info@npcmed.ru |
 | Москва, ул. Авиаторов, д. 38 |
О центре
Успешная имплантация стимуляторов диафрагмальных нервов ребёнку с редким заболеванием
В отделении реанимации и интенсивной терапии ГБУЗ «НПЦ спец.мед.помощи детям ДЗМ» успешно завершен длительный курс лечения четырехлетней девочки с редким, но очень тяжелым заболеванием: синдромом ROHHAD (Rapidonset Obesitywith Hypothalamicdysfunction, Hypoventilationand Autonomic Dysregulation). Этот синдром является крайне редким заболеванием, поразившим около 77 человек по всему миру, которое представляет собой внезапное ожирение, вызванное дисфункцией гипоталамуса, гиповентиляцию легких и автономную дисрегуляциию.
У больных ROHHAD поражается участок мозга, отвечающий за самостоятельное дыхание (пациент перестает дышать, уровень углекислого газа в крови повышается, но он не чувствует этого: не начинает задыхаться, не чувствует недомогания). Это заболевание является практически неизлечимым и потенциально смертельным. Больные обречены пожизненно находиться на искусственной вентиляции легких либо в больнице, либо в домашних условиях.
До 2-хлетнего возраста наша пациентка развивалась как все дети, но затем, в течение нескольких недель, набрала лишний вес с развитием тяжелого ожирения и дыхательных нарушений. В течение короткого периода самостоятельное дыхание стало неэффективным и девочка попала в одну из Московских больниц, где ее подключили к аппарату ИВЛ, позже наложили трахеостому и она была обречена пожизненно находиться на искусственной вентиляции легких и страдать от всех побочных эффектов этого лечения.
Несколько месяцев назад девочка была переведена в отделение реанимации и интенсивной терапии нашего Центра, где ей был проведен комплекс лечебных мероприятий в результате которых удалось снизить зависимость от аппарата ИВЛ, перевести ее на неинвазивную искусственную вентиляцию лёгких и закрыть трахеостому.
Следующим этапом было выполнено хирургическое лечение, ребенку были имплантированы стимуляторы диафрагмальных нервов, которые позволили полностью отказаться от аппарата ИВЛ. Оперирующий хирург А.Б. Сулейманов с ассистентами Голованевым П.С. и Асадовым Р.Н. при помощи нейрофизиологов Лапшиной Н.В. и Марынкиной А.Н., а так же анестезиолога Кочкина В.С. смогли последовательно, в ходе одной операции, установить два стимулятора диафрагмальных нервов справа и слева. После полного заживления послеоперационных ран, под руководством заведующего отделением реанимации Прокопьева Г.Г. были включены один за другим оба стимулятора и после 2 лет ИВЛ ребенок задышал без помощи аппарата искусственной вентиляции.
Это уже восьмой ребенок, прооперированный в ГБУЗ «НПЦспец.мед.помощи детям ДЗМ», которому установлены стимуляторы диафрагмальных нервов. Успех этого метода лечения обусловлен слаженной работой всех специалистов нашего Центра, накопленным большим опытом лечения детей с дыхательной недостаточностью и сотрудничеством с передовыми зарубежными медицинскими центрами, что позволяет внедрять в практику НПЦ самые современные методы лечения.
Стимулятор диафрагмального нерва что это такое
Икота встречается часто и происходит обычно случайно. Только при наличии множественных или длительных эпизодов икота, или сингультус, считается патологической. Неизвестно, играет ли она физиологическую роль. (Окончание. Начало материала здесь.)
Этиология
Икоту можно классифицировать, исходя из продолжительности. Длительностью более 48 часов классифицируется как стойкая, более 1 месяца — неукротимая.
Икота опосредуется рефлекторной дугой, состоящей из афферентных блуждающих, диафрагмальных и симпатических нервов с центром в стволе головного мозга, эфферентных нервов мышц диафрагмы и межреберных мышц. Вызвать ее могут патология или раздражение одной из ветвей этой рефлекторной дуги. Некоторые факты были хорошо задокументированы. Например, икота, вызванная инсультом, исчезла после лечения антикоагулянтами. Также был описан успешный исход после терапии менингита (Mandalà M. et al., 2010; Delèvaux I. et al., 2005; Sugimoto T. et al., 2008).
Не только повреждение соответствующих нервов может вызывать икоту, но и надпороговый раздражитель. Например, растяжение пищевода или желудка воздухом, пищей, употребление горячих жидкостей, а также гастроэзофагеальный рефлюкс и стенокардия (Fass R. et al., 1997; Pooran N. et al., 2006; Redondo-Cerezo E. et al., 2008; Kobayashi Z. et al,, 2009). Также было описано, что икота развивалась у пациентов с раком пищевода, после размещения стента в пищеводе, бронхоскопии, гастроскопии и во время электрической стимуляции левого предсердия (Turkyilmaz A., Eroglu A., 2008; Doshi H. et al., 2008). Длительная икота может быть вызвана инородным телом в ухе, присутствовать при опухолях шеи, неврологических расстройствах, диабете, уремии, алкоголизме и воспалительных или неопластических процессах в груди, таких как туберкулез, плеврит и рак. Гастроинтестинальные причины включают ГЭРБ и частичную непроходимость желудка.
Причины неукротимой икоты
♦ Стимуляция периферических нервов
Гастроинтестинальные:
сердечно-сосудистые:
локальное сжатие нерва:
местная инфекция нерва (герпес);
легочные:
♦ Центральная нервная система
♦ Системные факторы
Патогенез
Икота возникает в результате перемежающихся и принудительных спастических сокращений дыхательных мышц, что приводит к слышимым звукам.
Клиника
В большинстве случаев эпизоды икоты короткие и проходят спонтанно. Хроническая определена как длящаяся более 48 часов. Длительная и персистирующая икота может присутствовать в течение дней, месяцев и даже лет, создавая проблемы хронической слабости, расстройства сна, депрессии, потери веса и даже суицида.
Диагностика
Анамнез: другие симптомы и их продолжительность, использование лекарств, употребление наркотиков.
Физикальное обследование полное, включая уши, горло и нос; неврологическая оценка.
Лабораторные исследования включают общий анализ крови, на электролиты, мочевину, кортизол, амилазу, липазу, С-реактивный белок, функциональные пробы печени.
Инструментальные исследования: верхняя эндоскопия, ларингоскопия, ЭКГ, рентген и/или КТ грудной клетки и живота. В качестве последней надежды выступает МРТ головного мозга. Однако, как и манометрия пищевода, и 24-часовое измерение импеданса и рН, МРТ не всегда показана и может выполняться при наличии дополнительных симптомов или признаков. В большинстве случаев причины обнаружить не удается. Для оценки движения диафрагмы может быть выполнена флюороскопия.
Лечение
Большинство эпизодов икоты являются временными и саморазрешающимися и, возможно, вовсе не нуждаются в оценке или лечении. Когда икота начинается во время инвазивных процедур, таких как бронхоскопия, гастроскопия или во время инфузии анестетиков или химиотерапии, основная причина легко идентифицируется, и лечение должно быть направлено на нее. Если основная патология излечима, проблему можно решить. Но иногда действующий фактор не обнаруживается.
Аэрофагия
При этом функциональном расстройстве пациенты так часто проглатывают воздух и в таких больших количествах, что это приводит к появлению симптомов. Часть проглоченного воздуха вентилируется через желудочные отрыжки, а часть достигает кишечника, где вызывает вздутие живота.
Клинические симптомы многообразны — вплоть до опасных степеней растяжения просвета. Были описаны некоторые случаи у детей с психическими расстройствами, когда экстремальные объемы проглатываемого воздуха приводили к крайней дилатации желудка и кишечника с последующим заворотом желудка, илеусом и затруднениями дыхания (van der Kolk M. B. еt al., 1999; Komuro H. еt al., 2005; Frye R. E., Hait E. J., 2008).
Вздутие живота — частый симптом у пациентов с синдромом раздраженной кишки, функциональной диспепсией и запором. Но аэрофагия у них встречается очень редко.
Физиология
Проглатывание воздуха во время еды и питья — нормальный физиологический акт. В исследовании здоровых лиц, проглатывающих 10 мл жидкости, показано, что при этом захватываются 8–32 мл воздуха (Pouderoux P. et al., 1996). В вертикальном положении он скапливается в проксимальном отделе желудка. Растяжение свода последнего вызывает транзиторную релаксацию НПС, что позволяет воздуху выходить. Проглатывание напитков, содержащих углекислый газ, провоцирует отрыжку по тому же механизму (Tew S. et al., 2000). Как только воздух прошел НПС и поступил в тело пищевода, растяжение последнего приводит к расслаблению ВПС, что позволяет воздуху направляться в глотку.
Большинство людей со значительной отрыжкой полагают, что это следствие некоего рода органического заболевания. Часто пациенты убеждены, что у них необычно высокая продукция газа в желудке или кишечнике. У лиц с нормальной когнитивной функцией аэрофагия ассоциируется с ГЭРБ и грыжей пищеводного отверстия диафрагмы, но такая связь подтверждена плохо. Хроническая аэрофагия у детей может приВести к растяжению петель кишечника с истончением мускулатуры передней брюшной стенки.
Клиника
Другими симптомами являются метеоризм, абдоминальная или эпигастральная боль и запор. Желудочная отрыжка обычно не является преобладающим признаком, а наджелудочная вообще не наблюдается у пациентов с аэрофагией.
Нюансы:
Диагностика
Согласно третьему Римскому консенсусу, идентификация пациента с аэрофагией должна включать по крайней мере два следующих критерия:
Анамнез. Аэрофагию можно установить с помощью опроса. Вздутие, отрыжка, метеоризм, растяжение брюшной стенки, запор, абдоминальная боль, нет рвоты.
Физикальное исследование: увеличенный тимпанит по животу, нормальные кишечные звуки, никаких признаков илеуса; может быть после жевания жевательной резинки или курения.
Лабораторные исследования: полный анализ крови, скорость оседания эритроцитов, С-реактивный белок, функциональные тесты почек и печени, тестирование целиакии, радиоиммуносорбентный и радиоаллергосорбентный тесты, биохимические показатели железа, анализ на кальпротектин, анализ мочи.
Инструментальные исследования. Рентген живота. Растяжение кишечника, большой объем воздуха в кишечнике, отсутствие уровней газ/жидкость. Верхняя эндоскопия по усмотрению.
Наиболее удовлетворительным диагностическим критерием является вздутие живота, которое постепенно увеличивается в течение дня (минимальное рано утром и максимальное к концу вечера), усиление метеоризма во время сна и кишечных звуков при аускультации растянутого живота. Рентгенограмма, сделанная в конце дня, показывает растянутый воздухом желудок и нарастание объема газа в тонкой и толстой кишке без признаков обструкции.
Дифференциальная диагностика с механической непроходимостью может быть затруднена. Около 30 % пациентов после поступления в отделение неотложной помощи подвергались негативной диагностической лапаротомии (Bredenoord A. J., 2013). При ретроспективном осмотре рентгенограмм живота были только растянутые кишечные петли, но не уровни воздуха и жидкости, следовательно, признаки обструкции отсутствовали. Таким образом, у этих пациентов нужно избегать лапаротомии (Bredenoord A. J., 2013).
При синдроме раздраженной толстой кишки и запоре также может быть обнаружен увеличенный объем воздуха в кишечнике, однако не наблюдается повышенного проглатывания воздуха (Bredenoord A. J., 2013).
Лечение
Основывается главным образом на экспертном заключении, поскольку нет контролируемых исследований. Для лечения рекомендуется дифференциация пациентов с хроническими стабильными симптомами от пациентов с острыми и тяжелыми эпизодами аэрофагии, которые могут приВести к угрожающей ситуации. Последнее происходит преимущественно при психических отклонениях и может способствовать появлению заворота, непроходимости и затруднению дыхания из-за увеличения давления в брюшной полости. В этом случае постановка назогастрального зонда для эвакуации воздуха из желудка кажется разумной, а седативные средства, такие как лоразепам, могут помочь уменьшить повторное глотание воздуха (Bredenoord A. J., 2013).
У большинства пациентов симптомы хронические, и у них оправдан другой подход. Целесообразно ограничить потребление газированных напитков и медленно есть. Такие препараты, как эспумизан, предотвращают образование газов в кишечнике и могут облегчать симптомы. В случае запора, вторичного к растяжению тонкой и толстой кишки, указывается использование слабительных средств (Bredenoord A. J., 2013).
Диафрагмальный стимулятор
Диафрагмальный стимулятор представляет собой специальный медицинский прибор, оснащенный электродами, цель которого – посылать электрические импульсы на диафрагму. Используется диафрагмальный стимулятор при заболеваниях позвоночника, которые становятся причиной нарушения функционирования органов дыхательной системы, в частности, дисфункции диафрагмы.
Установка стимулятора
Диафрагмальный стимулятор оснащен 4 электродами, которые устанавливаются в мышечные волокна диафрагмы, 1 электродом, предназначенным для вживления в кожу, коннектором, скрепляющим электроды, фиксатором, который закрепляет коннектор на коже и импульсным генератором, находящимся снаружи.
Устанавливается диафрагмальный стимулятор лапароскопическим методом, через небольшие проколы, которые после операции закрываются косметическими швами. Проводится операция под контролем УЗИ, что дает хирургу выбрать на диафрагме оптимальное место для установки стимулятора. Проходит установка имплантата под общим наркозом.
Отсутствие необходимости в полостных разрезах значительно сокращает реабилитационный период, риски осложнений минимальные, после установки диафрагмального стимулятора возможно появление временного болевого симптома средней интенсивности.
Диафрагмальный стимулятор имплантируется в следующих случаях:
На 3 сутки после вживления стимулятора происходит установка наружного генератора и его соединение к электродам. В течение 2-3-х недель идет привыкание пациента к прибору, обучение его функционированию, корректировка работы прибора исходя из индивидуальных особенностей организма. Реабилитация и обучение использования прибора происходит в дневном стационаре под присмотром медицинского персонала. При наличии у пациента дыхательной недостаточности, что проявляется во время ночного сна, может потребоваться вентилирование легких неинвазивным методом.







