Стабилизация при онкологии что это такое и последствия
Как организовать жизнь после рака
Ремиссия при онкологических заболеваниях – это состояние, при котором все симптомы патологии пропадают и дальнейшее развитие опухоли не происходит.
Обычно под выздоровлением понимают пятилетнюю выживаемость после рака. При этом, у человека в течение пяти лет не должно появиться никаких симптомов опухоли, а также она не должна определяться на диагностических исследованиях. Такое состояние называют устойчивой ремиссией. По сути, тут врачи слегка перестраховываются и редко используют термин «выздоровление». Ведь гарантировать уничтожение всех без исключения раковых клеток в организме пока, увы, невозможно. Однако ремиссия на протяжении пяти и более лет – достаточно надежное тому подтверждение.
Каждый пациент должен четко знать, что возвращение к нормальной и полноценной жизни после рака возможно и даже необходимо. Но для этого ему потребуется несколько скорректировать привычки и крайне внимательно следить за состоянием здоровья.
Страхи выздоровевших пациентов
Разумеется, это, прежде всего, опасение, что болезнь вернется, страх рецидива после рака. Побороть его поможет четкое соблюдение рекомендаций врача, нужной диеты и распорядка дня. Однако если страх нарастает, приводя к развитию навязчивой тревожности и фобии – это уже серьезная проблема. Она может провоцировать ненужные самоограничения, создавать трудности во взаимоотношениях с окружающими и т.д. Решить эту проблему поможет обращение к профессиональному психологу.
Возвращение к нормальному образу жизни
Появятся ли у пациента, перенесшего онкозаболевание, какие-либо ограничения? Вполне возможно. Например, современное лечение рака нередко предполагает использование масштабных хирургических вмешательств. В зависимости от того, какой именно орган или его часть были удалены, может понадобиться определенная коррекция образа жизни человека, а также специальные уходовые процедуры.
Универсальные советы врачей
Вне зависимости от типа злокачественной патологии основой успешной реабилитации после рака специалисты считают:
Физические нагрузки
Опухолевые заболевания практически всегда сопровождаются синдромом повышенной усталости. Эффекты, связанные с плохим общим самочувствием, могут преследовать пациента еще некоторое время после завершения лечебного курса. И избавиться от таких проблем можно как раз с помощью физических упражнений.
Разумеется, вся активность должна быть строго дозирована, а увеличивать или корректировать ее должен специалист по лечебной физкультуре. Кроме того, очень важно, чтобы пациент имел достаточное время не только для труда, тренировок и бытовых забот, но и для полноценного отдыха. Данные многочисленных исследований доказывают, что те пациенты, которые проходят индивидуальные тренировочные программы и регулярно подвергают свой организм адекватным физическим нагрузкам, намного скорее возвращаются к полноценному образу жизни.
Благодаря правильно дозированной активности можно:
Питание
И во время, и после лечения пациенты должны уделять особенное внимание тому, какие продукты входят в их ежедневный рацион. При этом необходимо помнить, что применяемые в онкологии фармакологические препараты могут в значительной степени влиять на изменение вкусовых ощущений. Кроме того, одним из распространенных побочных эффектов этих лекарственных средств служит снижение аппетита, а также появление тошноты.
Однако подобные нарушения носят временный характер и после окончания курса лечения будут постепенно ослабевать вплоть до полного исчезновения. Но, пока они не пропали, лучше стараться разбить приемы пищи на несколько небольших порций, а для выбора блюд обратиться к профессиональному диетологу. Он поможет составить сбалансированный рацион, со всеми необходимыми для правильного обмена веществ элементами. И при этом учитываются индивидуальные особенности пациента, в том числе сложность перенесенного заболевания.
Вредные привычки
Конечно же, человеку необходимо избавиться от привычек, наносящих вред его здоровью, таких как употребление спиртных напитков и табакокурение. Они повышают риск развития рецидивов, усиливают побочные эффекты фармакологической терапии и значительно удлиняют период восстановления после онкологии.
Психологическая поддержка
Нередко всплеск эйфории и радости после победы над злокачественным заболеванием со временем переходит в некое разочарование, человек с трудом находит себе занятие, ему все кажется малозначимым. Таким пациентам потребуется, в первую очередь, помощь родных и близких, которые заново покажут ему ценность отношений, красоты мира и вызовут интерес к жизни. Иногда в таких случаях будет полезно и вмешательство психолога.
Профилактические скрининги
Важнейшее значение в жизни после рака имеют меры, направленные на предотвращение повторного развития заболевания. Ведущую роль играет регулярное посещение консультаций специалиста и прохождение медицинских обследований, согласно разработанному лечащим врачом графику.
Не меньшей значимостью обладают также и самостоятельные осмотры доступных частей тела: кожных покровов, слизистых оболочек, мягких тканей (например, молочной железы). К сожалению, уже случившийся эпизод онкологического заболевания означает, что вероятность появления другой злокачественной патологии у данного человека повышена. Теперь он автоматически относится к группе риска.
Соблюдение всех врачебных рекомендаций, здоровый образ жизни, сбалансированная диета и адекватные физические нагрузки помогут справиться со всеми последствиями раковой опухоли и в кратчайшие сроки вернуться к полноценной жизни.
Материал подготовлен по согласованию с врачом «Анадолу» медицинским онкологом Синаном Караасланом.
Как в фильмах не будет: что должен знать о химиотерапии каждый пациент
Химиотерапия — страшно и невыносимо. Об этом говорит нам медиапространство, и неудивительно, что из-за такой гиперболизации многие пациенты боятся ее едва ли не больше, чем самого заболевания. Однако ни один фильм и ни один роман не рассказывает, что это такое, как работает и насколько оправдан страх лекарственного лечения. Вместе с химиотерапевтом клиники «Луч» и научным сотрудником СПбКнПЦСВМП(о) Марией Степановой мы составили инструкцию для пациентов и разобрались, что такое лекарственная терапия и от чего зависит схема лечения.
Что такое лекарственное лечение
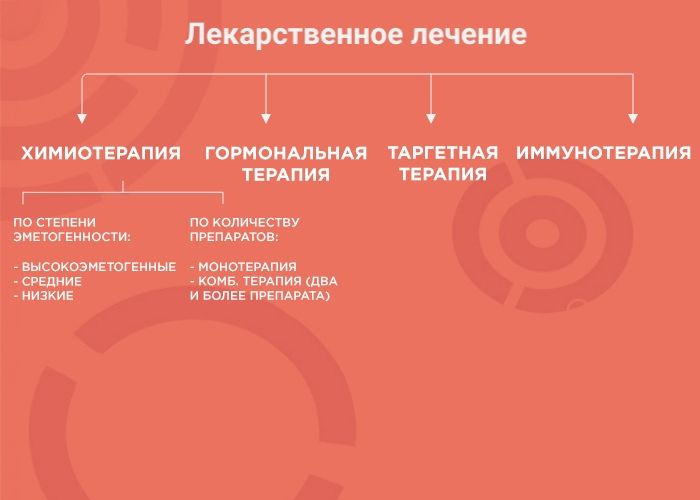
Лекарственная терапия — один из вариантов лечения онкологических заболеваний. Ее возможности и эффективность зависят от типа злокачественного образования. В лекарственной терапии выделяется четыре вида: химиотерапия, наиболее изученный вид терапии; гормонотерапия; таргетная терапия (англ. target «цель, мишень») и иммунотерапия, самый молодой и мало изученный вид лечения. Чтобы понять, почему врач выбирает тот или иной вид терапии, давайте рассмотрим каждый из них более подробно.
Химиотерапия (ХТ)
Некоторые до сих пор ошибочно считают, что лекарственная терапия сводится исключительно к химиотерапии. Действительно, долгое время лекарственное лечение злокачественных опухолей отводилось цитостатикам, противоопухолевым препаратам, принцип действия которых — разрушение быстро делящихся клеток. В том числе — злокачественных.
— Для пациента, который беспокоится о выраженности тошноты важно знать, какие препараты входят в конкретно его схему лечения. Я всегда рассказываю об этом и при необходимости назначаю препараты для снижения побочных эффектов. Чаще всего это сочетание внутривенного и таблетированного вариантов противорвотных препаратов. Однако, плохое самочувствие может нагнать пациента уже дома, и тогда я обсуждаю это и назначаю препараты, которые он может принимать без надзора врача.
— Получается, как в фильмах бывает редко?
— Крайне редко! Конечно, мутить будет, и многие сравнивают это ощущение с токсикозом во время беременности. В таких случаях я рекомендую пить чай с имбирем, использовать жевательные резинки, карамель с кислым вкусом, соленые и кислые продукты.
При химиотерапии используют множество препаратов с разным механизмом действия, ориентированным под разные особенности опухоли. Поэтому врачи используют либо монотерапию (один препарат), либо комбинированное лечение (два и более препарата). Это позволяет усилить противоопухолевый эффект и уменьшить вероятность развития устойчивости опухоли к лечению.
Выделяют также чувствительные к ХТ опухоли (например, герминогенные опухоли, хорионкарциномы, лимфомы) и опухоли, малочувствительные к ХТ (меланома, некоторые виды сарком). Чтобы найти оптимальные варианты лечения для увеличения продолжительности жизни, сейчас активно ведутся клинические исследования о возможности комбинировать этот вид терапии с иммунотерапией.
Гормональная терапия (ГТ)
При гормональной терапии применяются препараты, подавляющие выработку в организме его естественных гормонов или их взаимодействие с рецепторами. Самый частый вариант опухоли, где применяется данный вариант лечения, — рак молочной железы (РМЖ). При выполнении иммуногистохимического (ИГХ) исследования и наличии положительных рецепторов эстрогена и/или прогестерона, оптимальной опцией лечения является гормонотерапия. С ее помощью, можно остановить опухолевый рост и даже добиться полного или частичного исчезновения опухоли.
— Особенность применения этих препаратов, в том что они в подавляющем случае в таблетированной форме и имеют приемлемую токсичность по сравнению с ХТ. Это позволяет пациентам совмещать лечение с работой, хобби и путешествиями.
Таргетная терапия (ТТ)
В отличие от ХТ таргетные (целенаправленные) препараты атакуют только опухолевые клетки. Опухоль для ТТ — своего рода мишень, уничтожение которой означает прекращение репликации (воспроизведения) клеток и метастазирования.
Все началось с того, что врачи отметили недостаточный эффект от цитостатиков и начали внедрять иммуногистохимические параметры. Иммуногистохимическое исследование (ИГХ) выявляет в образце ткани белки, специфичные для того или иного вида клеток. Это позволяет отличать один вид опухоли от другого и выявлять маркеры, которые отвечают за лекарственную чувствительность опухолевой ткани.
— Таргетная терапия начинается с немелкоклеточного рака легкого: в порыве клинических исследований врачи разработали препарат, который начали применять в рамках клинических исследований. Широкое использование Ирессы в клинической практике сопровождалось преимущественно разочарованиями, связанными с редкостью проявления лечебного эффекта. Загадка разрешилась достаточно быстро: анализ нуклеотидной последовательности гена EGFR, проведенный тремя независимыми исследовательскими коллективами, установил, что опухоли легких, характеризующиеся чувствительностью к Ирессе или Тарцеве, содержат мутированную форму этого рецептора. Таким образом, с 2009 года Ирессу внедрили в клиническую практику для пациентов имеющих мутацию в гене EGFR. Особенность механизма действия ТТ, заключается в блокировании мутации, в результате чего опухоль не может делиться, — поясняет Мария.
Побочные эффекты при таргетной терапии менее выражены, и пациенту чаще всего не нужно находиться в стационаре. Некоторые таргетные препараты используются в таблетированной форме, во время их приема качество жизни пациента значительно не страдает, и пациенты могут вести привычный образ жизни.
Иммунотерапия (ИТ)
Иммунотерапия — самая молодая отрасль лекарственного лечения. Существует несколько групп иммунопрепаратов с разными механизмами действия. Одни воздействуют на звено образования кровеносных сосудов в опухоли и блокируют их развитие (после чего опухоль перестает получать питание и погибает), а другие активируют и направляют иммунные силы организма на борьбу с опухолью. занимает много времени, имеет свой спектр побочных эффектов, а также требует внимания врачей и тщательной оценки динамики состояния пациента.
— По идее мы с помощью введения препаратов обучаем иммунную систему распознавать клетки опухоли и разрушать их. Это все равно что установить антивирус, — объясняет Мария.
Цели и оценка эффективности лекарственного лечения
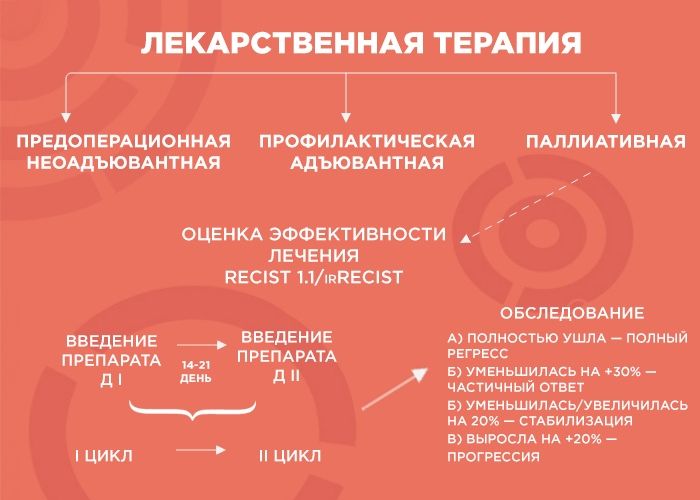
Лекарственная терапия бывает трех видов: предоперационная (неоадъювантная), профилактическая (адъювантная) и паллиативная (поддерживающая).
— Как проходит лечение в каждом из случаев?
— Начнем с предоперационной лекарственной терапии. Например, в отделение поступает пациент с диагнозом рак желудка. Результаты КТ показывают, что отдаленных метастатических очагов нет, однако в связи с распространением первичной опухоли операция на первом этапе невозможна. В этом случае лечение выглядит так: четыре курса терапии, затем — операция, а после нее — еще четыре курса адъювантной терапии. Зачем еще? Формально опухоль убрали, но есть риск возврата образования, и адъювантная терапия помогает его отсрочить.
Паллиативную терапию врач выбирает, когда хирургические методы бессильны (например, при отдаленных метастазах в легкие, печень, лимфоузлы и т.д.). Тогда лечение, в первую очередь, направлено на поддержание качества жизни пациента и контроль заболевания, и продолжительность лечения зависит от его эффекта. В химиотерапии врачи пользуются REСIST 1.1 — системой критериев оценки ответа опухоли на терапию, а в иммунотерапии — irRECIST.
— Объясню, как это работает, на примере пациента с опухолью толстой кишки и с множественными метастазами в печени и легких. Чтобы оценить серьезность ситуации, мы проводим обследование, выявляем наиболее измеряемые очаги и проводим два-три цикла химиотерапии. Большая часть курсов ХТ — введение препарата. Между первым введением и вторым — 14-21 дней — и этот временной промежуток называется циклом.
Далее мы смотрим и сравниваем. Если опухоль уменьшилась более чем на 30% — это частичный ответ, и нужно продолжать терапию до шести курсов. Если она ушла — это полный регресс, и тоже добавляем четыре курса, чтобы закрепить результат. Если опухоль увеличилась или уменьшилась на 20% — это стабилизация, мы делаем еще два курса и снова смотрим: если ситуация не изменилась, пациент отправляется на химиотерапевтические каникулы до прогрессирования заболевания, а потом схема повторяется.
Но если опухоль на фоне лечения выросла больше чем на 20% — мы имеем дело с прогрессией, вероятнее всего, это говорит нам об агрессивности опухоли. В этом случае я объясняю пациенту, что с ним происходит и почему мы меняем лечение.
— Как уговорить пациента на лечение?
— К каждому нужен индивидуальный подход. Я всегда говорю: «Химия может ухудшить ваше состояние, но бояться этого не стоит — мы попытаемся подобрать оптимальную симптоматическую терапию, которое уменьшит нежелательные явления». Если после этого во время лечения появятся данные о плохой переносимости, мы подумаем об уменьшении дозы цитостатика. Бывают случаи, когда я буквально уговариваю пациента пойти на терапию и объясняю ему, за что мы боремся. И объясняю это вне зависимости от серьезности случая — если при агрессивной опухоли человек настроен бороться до последнего, моя обязанность ему эту возможность дать.
Лучевая терапия при лечении рака: виды лечения, последствия.
Показания к лечению
Лучевая терапия при лечении рака: виды лечения, последствия.
Известно, что основными методами лечения различных злокачественных новообразований являются хирургический, лекарственный, лучевой и их сочетание. При этом операция и облучение считаются методами локального воздействия на опухоль, а лекарственная терапия (химиотерапия, таргетная терапия, гормонотерапия, иммунотерапия) – системным. Ассоциация онкологов во всем мире проводит различные многоцентровые исследования, призванные ответить на вопрос: «Какому методу или их сочетанию следует отдать предпочтение в различных клинических ситуациях?» В целом, все эти исследования преследуют одну цель – увеличить продолжительность жизни больных с онкопатологией и улучшить ее качество.
Пациент должен быть проинформирован лечащим врачом о различных способах лечения, включая альтернативное воздействие. Например, больным ранним раком легкого с тяжелой сопутствующей патологией и абсолютными противопоказаниями к операции, вместо хирургического лечения можно предложить облучение новообразования (стереотаксическая лучевая терапия), так называемое, лечение рака без операции. Или, например, при определенных показаниях у больных раком печени, предстательной железы. Активно и успешно используется стереотаксическая лучевая терапия вместо операции при опухолях головного мозга, тем самым значительно снижая риск послеоперационных осложнений и ускоряя реабилитацию пациентов после лечения. В центре «ОнкоСтоп» решение о проведении лучевой терапии (ЛТ), как самостоятельного варианта, так и в составе комплексного лечения, принимается консилиумом специалистов.
Радиотерапия (radiotherapy) планируется с учетом ниже перечисленных факторов. Во-первых, это основной диагноз, т.е. локализация злокачественной опухоли и степень ее распространения в окружающие ткани и отдаленные органы. Во-вторых, это степень злокачественности, наличие лимфоваскулярной инвазии и других прогностических и предиктивных факторов, которые определяются при морфологическом, иммуногистохимическом и молекулярно-генетическом исследованиях. В-третьих, это наличие предшествующего лечения и его эффективность. И в четвертых, это, безусловно, общее состояние пациента, возраст, наличие и степень коррекции сопутствующей патологии и ожидаемая продолжительность жизни больного.
Действие лучевой терапии основано на ионизирующем облучении определенной зоны потоком частиц, которые способны повреждать генетический аппарат (ДНК) клетки. Особенно это выражено у активно делящихся клеток, так как они наиболее восприимчивы к повреждающим факторам. Происходит нарушение функций и жизнедеятельности раковых клеток, что в свою очередь останавливает их развитие, рост и деление. Таким образом, в результате радиотерапии злокачественная опухоль уменьшается в размерах вплоть до полного исчезновения. К сожалению, здоровые клетки, которые располагаются по периферии новообразования, также могут входить в зону облучения в разном объеме (в зависимости от вида используемой радиотерапии), что впоследствии отражается на степени их повреждения и развития побочных эффектов. После лечения или в перерывах между сеансами облучения здоровые клетки способны восстанавливать свои радиационные повреждения, в отличие от опухолевых. 
Виды лучевой терапии
Существуют несколько классификаций лучевой терапии. В зависимости от того, когда назначается радиотерапия, она подразделяется на: неоадъювантную (до операции), адъювантную (после операции) и интраоперационную. Целями неоадъювантного облучения являются уменьшение размеров опухоли, достижение операбельного состояния, снижение риска метастазирования по сосудам кровеносной и лимфатической системы в лимфатические узлы и отдаленные органы (например, при раке молочной железы, раке прямой кишки). Адъювантное облучение направлено на минимизацию риска возникновения местных рецидивов опухоли (например, при раке молочной железы, злокачественной опухоли головного мозга, кости). В каждом конкретном случае целесообразность назначения радиотерапии определяется индивидуально.
При выборе способа доставки дозы излучения радиотерапевт оценивает в первую очередь локализацию опухоли, ее размер, близость сосудов, нервов, критических органов. В связи с этим существуют 3 способа подведения дозы:
Рассмотрим каждый из этих видов радиотерапии более подробно.
1. ДИСТАНЦИОННАЯ ЛУЧЕВАЯ ТЕРАПИЯ
При дистанционной лучевой терапии на опухоль через кожу направляется один или несколько пучков ионизирующего излучения (генерируются линейным ускорителем), которые захватывают саму опухоль и рядом расположенные ткани, уничтожая клетки внутри основного опухолевого объема и клетки, рассеянные вблизи него. Облучение линейным ускорителем обычно проводится 5 раз в неделю, с понедельника по пятницу, на протяжении нескольких недель.
* Аппарат для проведения дистанционного лучевого лечения: линейный ускоритель Varian TrueBeam
Далее рассмотрим отдельные виды дистанционной лучевой терапии.
ТРЕХМЕРНАЯ КОНФОРМНАЯ ЛУЧЕВАЯ ТЕРАПИЯ (3D-CRT)
Как известно, организм каждого пациента уникален и опухоли также неодинаковы по форме, размеру и локализации. При трехмерной конформной лучевой терапии возможно учитывать все эти факторы. В результате использования этой методики наведение пучка становится точнее, а прилежащие к опухоли здоровые ткани получают меньше радиации и быстрее восстанавливаются.
ЛУЧЕВАЯ ТЕРАПИЯ С МОДУЛЯЦИЕЙ ИНТЕНСИВНОСТИ ПУЧКА
Лучевая терапия с модуляцией интенсивности пучка (IMRT) – это особый вид трехмерной конформной лучевой терапии, при котором можно еще больше снизить лучевую нагрузку на здоровые ткани рядом с опухолью при условии точной адаптации пучка излучения к форме новообразования. Облучение на линейном ускорителе с использованием IMRT позволяет разбить каждый пучок на множество отдельных сегментов, при этом интенсивность излучения в пределах каждого сегмента регулируется индивидуально.
ЛУЧЕВАЯ ТЕРАПИЯ ПОД КОНТРОЛЕМ ВИЗУАЛИЗАЦИИ
Лечение лучевой терапией под визуальным контролем (IGRT) – это тоже конформное облучение опухоли, при котором для наведения пучка ежедневно используются методы визуализации (например, компьютерная томография, ультразвуковое или рентгенологическое исследование), проводимые непосредственно в каньоне (специальное помещение, в котором происходит лечение) перед каждой процедурой. В связи с тем, что между сеансами облучения линейным ускорителем опухоль может смещаться (например, в зависимости от степени наполнения полого органа или в связи с дыхательными движениями), IGRT позволяет более точно «прицеливаться» в опухоль, сберегая окружающие здоровые ткани. В некоторых случаях врачи имплантируют в опухоль или близлежащие ткани маленький маркер, чтобы лучше визуализировать мишень облучения.
СТЕРЕОТАКСИЧЕСКАЯ ЛУЧЕВАЯ ТЕРАПИЯ
Стереотаксическая лучевая терапия – особый метод лечения, позволяющий подводить высокую дозу ионизирующего излучения с субмиллиметровой точностью, в отличие от классической лучевой терапии (вышеописанные методики). Это позволяет эффективно и безопасно облучать опухоли, различные по локализации и размерам (даже самые маленькие очаги), и сохранять от повреждающего действия радиации окружающие здоровые ткани. Кроме того, стереотаксическая лучевая терапия может использоваться для повторного облучения. Эффект от терапии оценивается через 2-3 месяца после ее завершения. Все это время доктор активно наблюдает за состоянием здоровья пациента.
Интересный факт: стереотаксическая лучевая терапия впервые была разработана для однократного облучения опухолей головного мозга, что называется стереотаксической радиохирургией (SRS). Кроме онкопатологий, радиохирургию можно применять в лечении доброкачественных опухолей (например, менингиома, невринома слухового нерва) и определенных неопухолевых неврологических состояний (например, невралгия тройничного нерва, не поддающаяся консервативным методам лечения). Эта методика облучения большинству людей известна под названием «Гамма Нож», «КиберНож».
* Установка для стереотаксической радиохирургии патологий головного мозга: Гамма-нож (Gamma Knife)
Лечение опухолей вне черепа (экстракраниальных локализаций) называется стереотаксической лучевой терапией тела (SBRT), обычно реализуется за несколько сеансов, используется при раке легкого, печени, поджелудочной железы, предстательной железы, почки, опухолях спинного мозга, скелета. В целом, применение стереотаксической лучевой терапии в лечении различных онкопатологий открывает новые возможности.
* Аппарат для проведения стереотаксической лучевой терапии новообразований любых локализаций: КиберНож (Accuray CiberKnife)
Лечение с помощью стереотаксической лучевой терапии на современном роботизированном аппарате «КиберНож» доступно в центре лучевой терапии «Онкостоп».
ПРОТОННАЯ ЛУЧЕВАЯ ТЕРАПИЯ.
Протонная терапия является особым видом дистанционной лучевой терапии, при которой используются протоны. Физические свойства пучка протонов позволяют радиотерапевту более эффективно снижать дозу радиации в близко расположенных к опухоли нормальных тканях. Имеет узкий спектр применения (например, при опухолях головного мозга у детей).
* Аппарат для проведения протонной лучевой терапии: Varian ProBeam
НЕЙТРОННАЯ ЛУЧЕВАЯ ТЕРАПИЯ.
Нейтронное облучение также является особым видом дистанционной лучевой терапии, при которой используется нейтронное излучение. В клинической практике широко не используется.
2. КОНТАКТНАЯ ЛУЧЕВАЯ ТЕРАПИЯ (БРАХИТЕРАПИЯ)
Контактная ЛТ подразумевает временное или постоянное размещение радиоактивных источников внутри опухоли или в непосредственной близости от нее. Существует две основные формы брахитерапии – внутриполостная и внутритканевая. При внутриполостной лучевой терапии радиоактивные источники размещаются в пространстве рядом с опухолью, например, в канале шейки матки, влагалище или трахее. При внутритканевом лечении (например, рака предстательной железы) радиоактивные источники устанавливаются непосредственно в ткани (в предстательную железу). Ещё один вариант брахитерапии – это аппликационная форма, когда источники размещаются на поверхности кожи в специальные индивидуально адаптированные аппликаторы (например, для лечения рака кожи). Брахитерапия может быть назначена как изолированно, так и в комбинации с наружным облучением.
В зависимости от методики контактной ЛТ, ионизирующее излучение может подводиться с высокой мощностью дозы (high dose rate, HDR) или низкой (low dose rate, LDR). При высокодозной брахитерапии источник излучения размещается в опухоль временно посредством (тонкой) трубки – катетера. Установка катетера – это хирургическая манипуляция, требующая анестезии. Курс лечения обычно реализуется за большое количество сеансов (фракций), в режиме 1-2 раза в день или 1-2 раза в неделю. При низкодозной брахитерапии радиоактивные источники могут устанавливаться в опухоль временно или постоянно, что также требует хирургического пособия, анестезии и кратковременного пребывания в стационаре. Пациенты, которым установлены постоянные источники, в первое время после облучения ограничены в своей повседневной жизни, однако со временем восстанавливаются и возвращаются к прежнему ритму.
“Зерно” с радиоактивным материалом, вживляемых в опухоль при брахитерапии
СИСТЕМНАЯ ЛУЧЕВАЯ ТЕРАПИЯ
В некоторых клинических случаях пациентам назначается системная лучевая терапия, при которой радиоактивные препараты вводятся в кровоток и затем распределяются по всему организму. Их можно вводить через рот (радиоактивные таблетки) или через вену (внутривенное введение). Например, капсулами радиоактивного йода (I-131) лечатся некоторые виды рака щитовидной железы. Внутривенное введения радиоактивных препаратов эффективно при лечении боли, обусловленной наличием костных метастазов, например, при раке молочной железы.
Различают несколько этапов ЛТ: подготовительный (предлучевой), лучевой и восстановительный (постлучевой). Рассмотрим более подробно каждый этап терапии.
Подготовительная стадия начинается с первичной консультации радиотерапевта, который определяет целесообразность проведения лучевой терапии и выбирает методику. Следующим шагом является разметка опухоли, расчет дозы радиоактивного облучения и его планирование, в котором участвует радиотерапевт, медицинский физик и рентгенолаборант. При планировании лучевой терапии определяются область облучения, разовая и суммарная дозы радиации, максимум ионизирующего излучения, который приходится на опухолевую ткань и окружающие ее структуры, оценивается риск побочных эффектов. При необходимости выполняется маркирование опухоли (т.е. в нее имплантируются специальные маркеры), помогающее в дальнейшем отслеживать ее при дыхании. В некоторых случаях разметка границ облучения осуществляется специальным маркером, который нельзя стирать с кожи до завершения лечения. Если разметка стерлась в результате неосторожного обращения или после гигиенических процедур, то ее следует обновить под контролем лечащего врача. Перед лечением необходимо защищать кожу от прямого попадания солнечных лучей, не использовать косметику, раздражающие вещества, антисептики (йод). При кожных заболеваниях, аллергических проявлениях целесообразна их коррекция. При планировании облучения опухолей головы и шеи необходимо вылечить больные зубы и заболевания полости рта (например, стоматит).
Непосредственно сам процесс облучения сложный, и проводится согласно индивидуальному плану лечения. Он состоит из фракций (сеансов) ЛТ. Длительность и расписание фракций облучения индивидуальна в каждом случае, и зависит только от плана, который был составлен специалистами. Например, при стереотаксической радиохирургии лечение составляет одну фракцию, а при дистанционной лучевой терапии курс длится от одной до нескольких недель и осуществляется в течение недели пять дней подряд. Затем следует два дня перерыва для восстановления кожных покровов после проведенного облучения. В некоторых случаях, суточную дозу радиотерапевт разделяет на 2 сеанса (утром и вечером). Облучение проходит безболезненно в специальном помещении – каньоне. Перед лечением проводится подробный инструктаж техники безопасности. Во время терапии пациент должен находится в каньоне в неподвижном состоянии, дышать ровно и спокойно, с больным поддерживается двусторонняя связь посредством громкоговорителя. Оборудование во время сеанса лечения может создавать специфический шум, что является нормальным и не должно пугать пациента.
*Каньон Центра лучевой терапии проекта «ОнкоСтоп»
На протяжении всего курса лечения необходимо придерживаться следующих рекомендаций.
Особенности лучевой терапии опухолей различных локализаций
При раке молочной железы лучевая терапия используется после органосохраняющего хирургического вмешательства или после мастэктомии по показаниям (наличие метастатических регионарных лимфатических узлов, опухолевые клетки в краях операционного материала и др.). Используемая дистанционная радиотерапия в этих случаях имеет цель элиминировать (уничтожить), возможно оставшиеся в ране опухолевые клетки, тем самым снижая риск локального рецидива. При местно-распространенном раке молочной железы облучение может быть назначено и до хирургического лечения с целью достижения операбельного состояния. Во время лечения женщин могут беспокоить такие жалобы, как утомляемость, отечность и изменение цвета кожи молочной железы (так называемое «бронзирование»). Однако, эти симптомы обычно исчезают сразу или в течение 6 месяцев после завершения лучевой терапии.
При лечении рака прямой кишки активно используют лучевую терапию до операции, поскольку она позволяет уменьшить объем операции и снизить риск метастазирования опухоли в дальнейшем (во время хирургического вмешательства и после него). Сочетание облучения и химиотерапии приводит к увеличению эффективности терапии этой категории пациентов.
При раке женских половых органов применяется как дистанционное облучение органов малого таза, так и брахитерапия. Если при I стадии рака шейки матки лучевая терапия может назначаться по определенным показаниям, то при II, III, IVA стадиях облучение совместно с химиотерапией является стандартом лечения этой когорты больных.
Восстановительный (постлучевой) период
Постлучевой период начинается сразу после окончания облучения. В большинстве случаев пациенты активно не предъявляют жалобы и чувствуют себя относительно удовлетворительно. Однако некоторых больных могут беспокоить побочные эффекты, которые различаются по степени своей выраженности в каждом конкретном случае. При появлении нежелательных реакций необходимо сразу обратиться к врачу.
Восстановительный период (реабилитация) заключается в соблюдении щадящего режима дня и полноценного питания. Важное значение имеет эмоциональный настрой больного, помощь и доброжелательное отношение к нему близких людей, правильное соблюдение предписанных рекомендаций (контрольное обследование).
Усталость при облучении обусловлена повышенным уровнем энергозатрат и сопровождается различными метаболическими изменениями. Поэтому, если пациент активно работает, то ему лучше перейти на легкий труд или уйти в отпуск для восстановления сил и здоровья.
После завершения курса лучевой терапии необходимо регулярно посещать врача для контроля за состоянием здоровья и оценки эффективности лечения. Динамическое наблюдение осуществляется онкологом в районной поликлинике, онкодиспансере, частной клинике по желанию больного. В случае ухудшения состояния здоровья, развития болевого синдрома, появлении каких-либо новых жалоб, связанных, например, с нарушением функции желудочно-кишечного тракта, мочеполовой системы, сердечно-сосудистых и дыхательных нарушений, повышением температуры тела, следует обращаться к врачу, не дожидаясь очередного запланированного визита.
Особую роль играет правильный уход за кожей, которая легко поддается повреждающему действию радиации (особенно при дистанционной лучевой терапии). Необходимо часто пользоваться питательным жирным кремом, даже в отсутствии признаков воспаления и ожога кожного покрова. В период облучения и после него нельзя посещать бани или ванны, пользоваться жесткими мочалками, скрабами. Лучше принимать душ и использовать мягкие питательные и увлажняющие косметические средства.
Многие считают, что пациенты, перенесшие лучевую терапию, могут сами излучать радиацию, поэтому им целесообразно минимизировать общение с окружающими людьми, особенно с беременными женщинами и детьми. Однако, это заблуждение. Облученные больные не представляют опасности для окружающих. Не стоит отказываться по этой причине и от интимных отношений. При изменении состояния слизистых оболочек половых путей и возникновении неприятных ощущений следует рассказать об этом врачу, он подскажет, как с этим бороться.
Некоторые больные испытывают стресс, в связи с чем необходимо правильно организовать свой досуг: кино, театр, музеи, выставки, концерты, встреча с друзьями, прогулки на свежем воздухе и различные общественные мероприятия на ваш выбор.
Лучевые повреждения кожи, такие как покраснение (со временем оно проходит, иногда оставляя после себя пигментацию), сухость, зуд, жжение, шелушение в зоне облучения. При правильном уходе кожные покровы восстанавливаются в течение 1-2 месяцев после лучевой терапии. В ряде случаев при выраженном лучевом повреждении развиваются ожоги разной степени выраженности, которые впоследствии могут инфицироваться.
Инфекционные осложнения, риск их возникновения повышается при сахарном диабете, наличии сопутствующей патологии кожи, при высокой дозе радиации, светлом типе кожи.
Чтобы избежать подобных осложнений, необходимо строго соблюдать предписанные рекомендации лечащего врача и правильно осуществлять уход за кожей.
Лучевые повреждения слизистой оболочки облучаемой области. Например, при облучении опухолей головы и шеи возможно повреждение слизистой полости рта, носа, гортани. В связи с этим, пациентам необходимо соблюдать некоторые правила:
При лучевом лечении опухолей прямой кишки может появиться склонность к запорам, примесь крови в кале, боль в области ануса и животе, поэтому важно соблюдать диету (исключить «закрепляющие» продукты).
При облучении органов малого таза больные могут предъявлять жалобы на расстройство мочеиспускания (болезненность, жжение, затруднение мочеиспускания).
Осложнения со стороны дыхательной системы: кашель, затрудненное дыхание, болезненность и отек кожи грудной стенки. Может наблюдаться при лучевой терапии опухолей грудной клетки, легкого, молочной железы.
О любом ухудшении самочувствия, появлении вышеперечисленных изменений, необходимо проинформировать об этом лечащего врача, который назначит соответствующее сопроводительное лечение согласно выявленным нарушениям.
В целом, лучевая терапия в большинстве случаев переносится пациентами хорошо, и после нее больные быстро восстанавливаются. Облучение является важным этапом в комплексном лечении злокачественных новообразований, позволяя с еще большей эффективностью воздействовать на опухоль, что в свою очередь приводит к увеличению продолжительности жизни больных и повышению ее качества.
Специалисты центра лучевой терапии проекта «ОнкоСтоп» успешно владеют всеми видами дистанционной лучевой терапии, включая стереотаксическую, и бережно заботятся о здоровье своих пациентов.