агрегатное состояние муки 5 класс
LiveInternetLiveInternet
—Метки
—Подписка по e-mail
—Статистика
19 агрегатных состояний вещества
Наиболее распространено знание о трех агрегатных состояниях: жидком, твердом, газообразном, иногда вспоминают о плазменном, реже жидкокристаллическом. Последнее время в интернете распространился перечень 17 фаз вещества, взятый из известной книги (ru) Стивена Фрая. Поэтому мы расскажем о них подробнее, т.к. о материи следует знать немного больше хотя бы для того, чтобы лучше понимать процессы, происходящие во Вселенной.
Приведённый ниже список агрегатных состояний вещества возрастает от самых холодных состояний к самым горячим и т.о. может быть продолжен. Одновременно следует понимать, что от газообразного состояния (№11), самого «разжатого», в обе стороны списка степень сжатия вещества и его давление (с некоторыми оговорками для таких неизученных гипотетических состояний, как квантовое, лучевое или слабо симметричное) возрастают.После текста приведен наглядный график фазовых переходов материи.
1. Квантовое — агрегатное состояние вещества, достигаемое при понижении температуры до абсолютного нуля, в результате чего исчезают внутренние связи и материя рассыпается на свободные кварки.
2. Конденсат Бозе-Эйнштейна — агрегатное состояние материи, основу которой составляют бозоны, охлаждённые до температур, близких к абсолютному нулю (меньше миллионной доли градуса выше абсолютного нуля). В таком сильно охлаждённом состоянии достаточно большое число атомов оказывается в своих минимально возможных квантовых состояниях и квантовые эффекты начинают проявляться на макроскопическом уровне. Конденсат Бозе-Эйнштейна (который зачастую называют «бозе-конденсат», или попросту «бэк») возникает, когда вы охлаждаете тот или иной химический элемент до чрезвычайно низких температур (как правило, до температуры чуть выше абсолютного нуля, минус 273 градуса по Цельсию, — теоретическая температура, при которой все перестает двигаться).
Вот тут с веществом начинают происходить совершенно странные вещи. Процессы, обычно наблюдаемые лишь на уровне атомов, теперь протекают в масштабах, достаточно крупных для наблюдения невооруженным глазом. Например, если поместить «бэк» в лабораторный стакан и обеспечить нужный температурный режим, вещество начнет ползти вверх по стенке и в конце концов само по себе выберется наружу.
Судя по всему, здесь мы имеем дело с тщетной попыткой вещества понизить собственную энергию (которая и без того находится на самом низком из всех возможных уровней).
Замедление атомов с использованием охлаждающей аппаратуры позволяет получить сингулярное квантовое состояние, известное как конденсат Бозе, или Бозе — Эйнштейна. Это явление было предсказано в 1925 году А. Эйнштейном, как результат обобщения работы Ш. Бозе, где строилась статистическая механика для частиц, начиная от безмассовых фотоно до обладающих массой атомов (рукопись Эйнштейна, считавшаяся утерянной, была обнаружена в библиотеке Лейденского университета в 2005 году). Результатом усилий Бозе и Эйнштейна стала концепция Бозе газа, подчиняющегося статистике Бозе — Эйнштейна, которая описывает статистическое распределение тождественных частиц с целым спином, называемых бозонами. Бозоны, которыми являются, например, и отдельные элементарные частицы — фотоны, и целые атомы, могут находиться друг с другом в одинаковых квантовых состояниях. Эйнштейн предположил, что охлаждение атомов — бозонов до очень низких температур заставит их перейти (или, по-другому, сконденсироваться) в наинизшее возможное квантовое состояние. Результатом такой конденсации станет возникновение новой формы вещества.
Этот переход возникает ниже критической температуры, которая для однородного трёхмерного газа, состоящего из невзаимодействующих частиц без каких-либо внутренних степеней свободы.
4. Сверхтекучее вещество — состояние, при котором у вещества фактически отсутствует вязкость, а при течении он не испытывает трения с твёрдой поверхностью. Следствием этого является, например, такой интересный эффект, как полное самопроизвольное «выползание» сверхтекучего гелия из сосуда по его стенкам против силы тяжести. Нарушения закона сохранения энергии здесь, конечно же, нет. В отсутствие сил трения на гелий действуют только силы тяжести, силы межатомного взаимодействия между гелием и стенками сосуда и между атомами гелия. Так вот, силы межатомного взаимодействия превышают все остальные силы вместе взятые. В результате гелий стремится растечься как можно сильнее по всем возможным поверхностям, поэтому и «путешествует» по стенкам сосуда. В 1938 году советский учёный Пётр Капица доказал, что гелий может существовать в сверхтекучем состоянии.
Стоит отметить, что многие из необычных свойств гелия известны уже довольно давно. Однако и в последние годы этот химический элемент «балует» нас интересными и неожиданными эффектами. Так, в 2004 году Мозес Чань и Эун-Сьонг Ким из Университета Пенсильвании заинтриговали научный мир заявлением о том, что им удалось получить совершенно новое состояние гелия — сверхтекучее твёрдое вещество. В этом состоянии одни атомы гелия в кристаллической решётке могут обтекать другие, и гелий таким образом может течь сам через себя. Эффект «сверхтвёрдости» теоретически был предсказан ещё в 1969 году. И вот в 2004 году — как будто бы и экспериментальное подтверждение. Однако более поздние и весьма любопытные эксперименты показали, что не всё так просто, и, возможно, такая интерпретация явления, которое до этого принималось за сверхтекучесть твёрдого гелия, неверна.
Эксперимент учёных под руководством Хэмфри Мариса из Университета Брауна в США был прост и изящен. Учёные помещали перевёрнутую вверх дном пробирку в замкнутый резервуар с жидким гелием. Часть гелия в пробирке и в резервуаре они замораживали таким образом, чтобы граница между жидким и твёрдым внутри пробирки была выше, чем в резервуаре. Иными словами, в верхней части пробирки был жидкий гелий, в нижней — твёрдый, он плавно переходил в твёрдую фазу резервуара, над которой был налито немного жидкого гелия — ниже, чем уровень жидкости в пробирке. Если бы жидкий гелий стал просачиваться через твёрдый, то разница уровней уменьшилась бы, и тогда можно говорить о твёрдом сверхтекучем гелии. И в принципе, в трёх из 13 экспериментов разница уровней действительно уменьшалась.
5. Сверхтвёрдое вещество — агрегатное состояние при котором материя прозрачна и может «течь», как жидкость, но фактически она лишена вязкости. Такие жидкости известны много лет, их называют суперфлюидами. Дело в том, что если супержидкость размешать, она будет циркулировать чуть ли не вечно, тогда как нормальная жидкость в конечном счёте успокоится. Первые два суперфлюида были созданы исследователями с использованием гелия-4 и гелия-3. Они были охлаждены почти до абсолютного нуля — до минус 273 градусов Цельсия. А из гелия-4 американским учёным удалось получить сверхтвёрдое тело. Замороженный гелий они сжали давлением более чем в 60 раз, а затем заполненный веществом стакан установили на вращающийся диск. При температуре 0,175 градусов Цельсия диск внезапно начал вращаться свободнее, что, по мнению учёных, свидетельствует о том, что гелий стал супертелом.
6. Твёрдое — агрегатное состояние вещества, отличающееся стабильностью формы и характером теплового движения атомов, которые совершают малые колебания вокруг положений равновесия. Устойчивым состоянием твердых тел является кристаллическое. Различают твердые тела с ионной, ковалентной, металлической и др. типами связи между атомами, что обусловливает разнообразие их физических свойств. Электрические и некоторые др. свойства твердых тел в основном определяются характером движения внешних электронов его атомов. По электрическим свойствам твердые тела делятся на диэлектрики, полупроводники и металлы, по магнитным — на диамагнетики, парамагнетики и тела с упорядоченной магнитной структурой. Исследования свойств твердых тел объединились в большую область — физику твердого тела, развитие которой стимулируется потребностями техники.
7. Аморфное твёрдое — конденсированное агрегатное состояние вещества, характеризующееся изотропией физических свойств, обусловленной неупорядоченным расположением атомов и молекул. В аморфных твердых телах атомы колеблются около хаотически расположенных точек. В отличие от кристаллического состояния переход из твердого аморфного в жидкое происходит постепенно. В аморфном состоянии находятся различные вещества: стекла, смолы, пластмассы и т. д.
9. Жидкое — агрегатное состояние вещества, сочетающее в себе черты твердого состояния (сохранение объема, определенная прочность на разрыв) и газообразного (изменчивость формы). Для жидкости характерны ближний порядок в расположении частиц (молекул, атомов) и малое различие в кинетической энергии теплового движения молекул и их потенциальной энергии взаимодействия. Тепловое движение молекул жидкости состоит из колебаний около положений равновесия и сравнительно редких перескоков из одного равновесного положения в другое, с этим связана текучесть жидкости.
11. Газообразное — (франц. gaz, от греч. chaos — хаос), агрегатное состояние вещества, в котором кинетическая энергия теплового движения его частиц (молекул, атомов, ионов) значительно превосходит потенциальную энергию взаимодействий между ними, в связи с чем частицы движутся свободно, равномерно заполняя в отсутствие внешних полей весь предоставленный им объем.
12. Плазма — (от греч. plasma — вылепленное, оформленное), состояние вещества, представляющее из себя ионизованный газ, в котором концентрации положительных и отрицательных зарядов равны (квазинейтральность). В состоянии плазмы находится подавляющая часть вещества Вселенной: звезды, галактические туманности и межзвездная среда. Около Земли плазма существует в виде солнечного ветра, магнитосферы и ионосферы. Высокотемпературная плазма ( Т
106 — 108К) из смеси дейтерия и трития исследуется с целью осуществления управляемого термоядерного синтеза. Низкотемпературная плазма ( Т Ј 105К) используется в различных газоразрядных приборах (газовых лазерах, ионных приборах, МГД-генераторах, плазмотронах, плазменных двигателях и т. д.), а также в технике (см. Плазменная металлургия, Плазменное бурение, Плазменная технология).
13. Вырожденное вещество — является промежуточной стадией между плазмой и нейтрониумом. Оно наблюдается в белых карликах, играет важную роль в эволюции звезд. Когда атомы находятся в условиях чрезвычайно высоких температур и давлений, они теряют свои электроны (они переходят в электронный газ). Другими словами, они полностью ионизованы (плазма). Давление такого газа (плазмы) определяется давлением электронов. Если плотность очень высока, все частицы вынуждены приближаться к друг другу. Электроны могут находится в состояниях с определенными энергиями, причем два электрона не могут иметь одинаковую энергию (если только их спины не противоположны). Таким образом, в плотном газе все нижние уровни энергии оказываются заполненными электронами. Такой газ называется вырожденным. В этом состоянии электроны проявляют вырожденное электронное давление, которое противодействует силам гравитации.
14. Нейтрониум — агрегатное состояние, в которое вещество переходит при сверхвысоком давлении, недостижимом пока в лаборатории, но существующем внутри нейтронных звёзд. При переходе в нейтронное состояние электроны вещества взаимодействуют с протонами и превращаются в нейтроны. В результате вещество в нейтронном состоянии полностью состоит из нейтронов и обладает плотностью порядка ядерной. Температура вещества при этом не должна быть слишком высока (в энергетическом эквиваленте не более сотни МэВ).
При сильном повышении температуры (сотни МэВ и выше) в нейтронном состоянии начинают рождаться и аннигилировать разнообразные мезоны. При дальнейшем повышении температуры происходит деконфайнмент, и вещество переходит в состояние кварк-глюонной плазмы. Оно состоит уже не из адронов, а из постоянно рождающихся и исчезающих кварков и глюонов.
15. Кварк-глюонная плазма (хромоплазма) — агрегатное состояние вещества в физике высоких энергий и физике элементарных частиц, при котором адронное вещество переходит в состояние, аналогичное состоянию, в котором находятся электроны и ионы в обычной плазме.
Обычно вещество в адронах находится в так называемом бесцветном («белом») состоянии. То есть, кварки различных цветов компенсируют друг друга. Аналогичное состояние есть и у обычного вещества — когда все атомы электрически нейтральны, то есть,
положительные заряды в них компенсированы отрицательными. При высоких температурах может происходить ионизация атомов, при этом заряды разделяются, и вещество становится, как говорят, «квазинейтральным». То есть, нейтральным остаётся всё облако вещества в целом, а отдельные его частицы нейтральными быть перестают. Точно так же, по-видимому, может происходить и с адронным веществом — при очень высоких энергиях, цвет выходит на свободу и делает вещество «квазибесцветным».
Предположительно, вещество Вселенной находилось в состоянии кварк-глюонной плазмы в первые мгновения после Большого Взрыва. Сейчас кварк-глюонная плазма может на короткое время образовываться при соударениях частиц очень высоких энергий.
Кварк-глюонная плазма была получена экспериментально на ускорителе RHIC Брукхейвенской национальной лаборатории в 2005 году. Максимальная температура плазмы в 4 триллиона градусов Цельсия была получена там же в феврале 2010 года.
19. Лучевое вещество — это, по сути дела, уже совсем не вещество, а в чистом виде энергия. Однако именно это гипотетическое агрегатное состояние примет тело, достигшее скорости света. Также его можно получить, разогрев тело до планковской температуры (1032К), то есть разогнав молекулы вещества до скорости света. Как следует из теории относительности, при достижении скорости более 0,99 с, масса тела начинает расти гораздо быстрее, нежели при «обычном» ускорении, кроме того тело удлиняется, разогревается, то есть начинает излучать в инфракрасном спектре. При пересечении порога 0,999 с, тело кардинально видоизменяется и начинает стремительный фазовый переход вплоть до лучевого состояния. Как следует из формулы Эйнштейна, взятой в полном виде, растущая масса итогового вещества складывается из масс, отделяющихся от тела в виде теплового, рентгеновского, оптического и других излучений, энергия каждого из которых описывается следующим членом в формуле. Таким образом, тело приблизившееся к скорости света начнет излучать во всех спектрах, расти в длину и замедляться во времени, утоньшаясь до планковской длины, то есть по достижении скорости с, тело превратится в бесконечно длинный и тонкий луч, двигающийся со скоростью света и состоящий из фотонов, не имеющих длины, а его бесконечная масса полностью перейдет в энергию. Поэтому такое вещество и называется лучевым.
Основные агрегатные состояния вещества
Агрегатные состояния вещества
Чтобы разобраться с тем, какими бывают агрегатные состояния, предлагаю по ходу чтения статьи заполнять таблицу.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
Лед, вода и водяной пар — это все три агрегатных состояния одного вещества. Лед — твердое состояние, вода — жидкая, пар — газообразное. Для каждого вещества существует три состояния.
Твердое состояние
Его очень легко представить — это любой предмет, который мы встречаем в жизни. В этом состоянии тело сохраняет форму и объем. Расстояние между молекулами, приблизительно равно размеру самих молекул, которые, в свою очередь, расположены очень структурированно.
Такая структура называется кристаллической решеткой — из-за четкой структуры молекулам сложно двигаться, и они просто колеблются около своих положений.
Заполняем нашу табличку
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
Жидкое состояние
В этом состоянии сохраняется объем, но не сохраняется форма. Например, если перелить молоко из кувшина в стакан, то молоко, имевшее форму кувшина, примет форму стакана. Кстати, в корове у молока тоже была другая форма.
Расстояние между молекулами в жидком состоянии чуть больше, чем в твердом, но все равно невелико. При этом частицы не собраны в кристаллическую решетку, а расположены хаотично. Молекулы почти не двигаются, но при нагревании жидкости делают это более охотно.
Вспомните, что происходит, если залить чайный пакетик холодной водой — он почти не заваривается. А вот если налить кипяточку — чай точно будет готов.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
Газообразное состояние
В жизни мы встречаем газообразное состояние вещества, когда чувствуем запахи. Запах очень легко распространяется, потому что газ не имеет ни формы, ни объема (он занимает весь предоставленный ему объем), состоит из хаотично движущихся молекул, расстояние между которыми больше, чем размеры молекул.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
занимают предоставленный объем
больше размеров молекул
хаотичное и непрерывное
С агрегатными состояниями разобрались, ура! Но до сих пор неясно, каким образом у каждого вещества их целых три, и как одно переходит в другое. Для этого узнаем, что такое фазовые переходы.
Фазовые переходы: изменение агрегатных состояний вещества
При изменении внешних условий (например, если внутренняя энергия тела увеличивается или уменьшается в результате нагревания или охлаждения) могут происходить фазовые переходы — изменения агрегатных состояний вещества.
Фазовые переходы интересны тем, что все живое не Земле существует лишь благодаря тому, что вода умеет превращаться в лед или пар. С кристаллизацией, плавлением, парообразованием и конденсацией связаны многие процессы металлургии и микроэлектроники.
На схеме — названия всех фазовых переходов:
Переход из твердого состояния в жидкое — плавление;
Переход из жидкого состояния в твердое — кристаллизация;
Переход из газообразного состояния в жидкое — конденсация;
Переход из жидкого состояния в газообразное — парообразование;
Переход из твердого состояния в газообразное, минуя жидкое — сублимация;
Переход из газообразного состояния в твердое, минуя жидкое — десублимация.
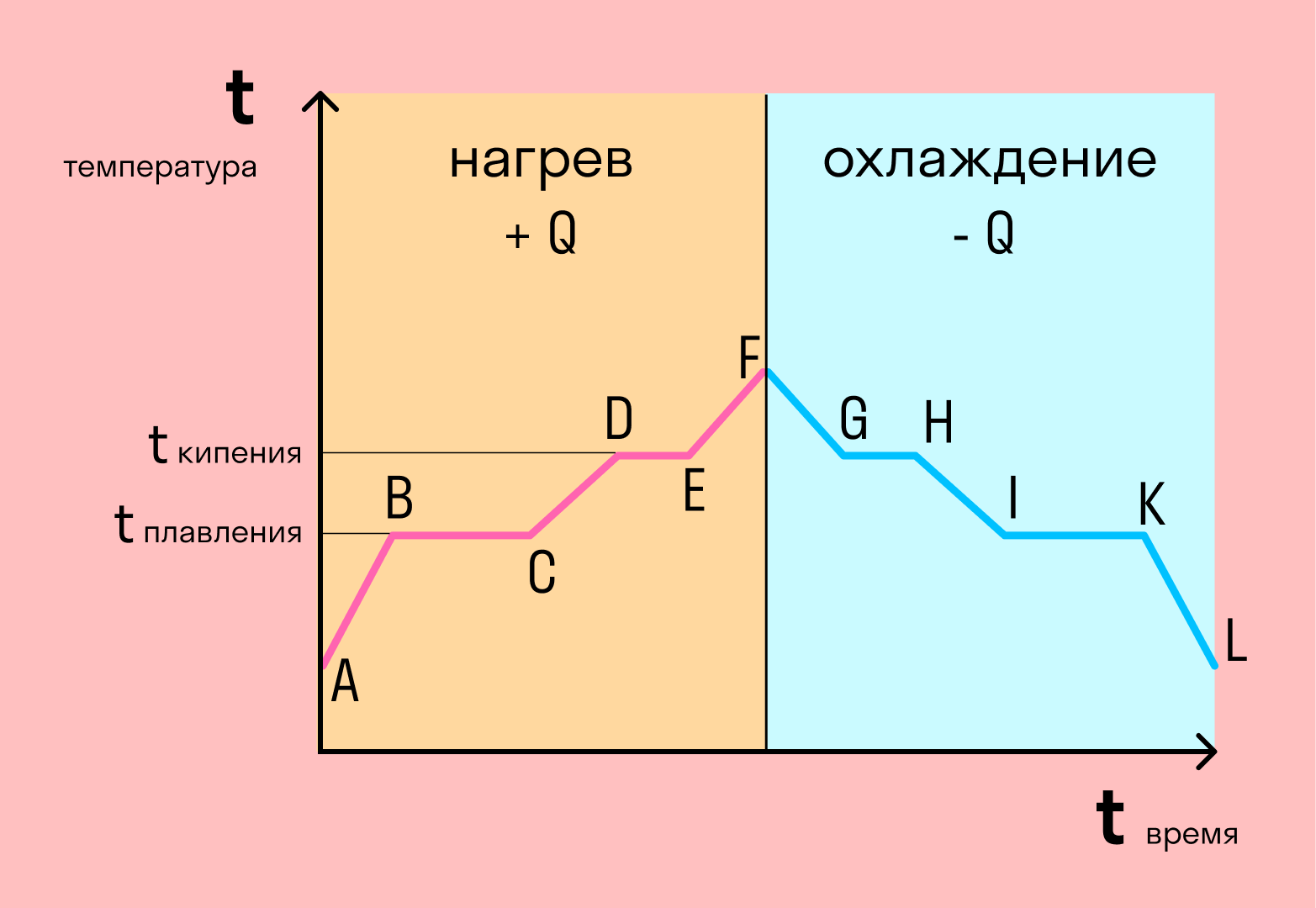
График фазовых переходов
Если взять процесс превращения льда в воду, воды — в пар, и обратные действия, то мы получим очень информативный график.
Разбираемся по шагам. Сначала взяли лед, конечно, при отрицательной температуре, потому что при нуле лед начинает плавиться. Нагрели лед до температуры плавления (до 0 градусов).
После того, как лед нагрелся до температуры плавления, он начинает плавиться. Плавление происходит при постоянной температуре тем дольше длится, чем больше масса плавящегося вещества. Еще этот процесс зависит от свойств самого вещества, но об этом немного позже.
Расправившись вещество уже в жидком состоянии снова начинает нагреваться, и температура увеличивается, пока не достигает температуры кипения. В данном случае нагревается вода — это значит, что ее температура кипения равна 100 градусам Цельсия.
При 100 градусах вода кипит, пока не выкипит целиком. В данном случае процесс аналогично плавлению происходит при постоянной температуре. Данный процесс нельзя путать с испарением, потому что парообразование происходит при конкретной температуре, а испарение — при любой.
Далее полученный пар нагревается, но путем нагревания невозможно дойти до другого фазового перехода — можно пойти только обратно.
Первый шаг в обратную сторону — охлаждение до температуры кипения.
Дойдя до температуры кипения (в данном случае 100 градусов), пар начинает переходить в жидкое состояние. Этот процесс также происходит при постоянной температуре.
Сконденсировавшись, вода охлаждается, пока не начнет замерзать.
Кристаллизуется (замерзает) вода при той же температуре, что и плавится лед — 0 градусов. Кристаллизация также происходит при постоянной температуре.
После кристаллизации лед охлаждается.
С нагреванием и охлаждением все совсем просто — мы либо передаем теплоту телу (веществу), и оно идет на увеличение температуры, либо тело отдает тепло и охлаждается.
В остальных процессах температура не меняется. Это связано с тем, что количество теплоты не всегда зависит от температуры. Формулы для всех процессов выглядят так:
Нагревание
Охлаждение
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
m — масса [кг]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
Плавление
Кристаллизация
Q — количество теплоты [Дж]
λ — удельная теплота плавления вещества [Дж/кг]
m — масса [кг]
Парообразование
Конденсация
Q — количество теплоты [Дж]
L — удельная теплота парообразования вещества [Дж/кг]
m — масса [кг]
Решение задач по фазовым переходам
С теорией разобрались — а теперь давайте практиковаться!
Задачка раз. Температура медного образца массой 100 г повысилась с 20 °С до 60 °С. Какое количество теплоты получил образец? Удельную теплоёмкость меди считать равной 380 Дж/(кг умножить на °С)
Q = 380 * 0,1*(60-20) = 1520 Дж
Ответ: образец получил 1520 Дж
Задачка два. Какое количество теплоты необходимо для плавления 2,5 т стали, взятой при температуре плавления? Удельная теплота плавления стали λ=80кДж/кг. Теплопотерями пренебречь.
80 кДж/кг = 80000 Дж/кг
Q = 80000*2500 = 200 000 000 Дж = 200 МДж
Ответ: для плавления 2,5 т стали необходимо 200 МДж теплоты.
Сублимация и десублимация
Мы уже рассказали про такие процессы, как сублимация и десублимация.
Примерчики из жизни🤓
Про принтеры. Цветные принтеры (только не лазерные) печатают путем сублимации. Вот как это работает: частицы краски быстро переходят из твердого состояния в газообразное и оседают на бумаге — так получается цветная картинка.
Рисуночки на окнах. Если вы решите проехаться на автобусе в холодную погоду — увидете на стеклах чудесные узоры. Из-за огромной разницы температур между улицей и автобусом, мы можем наблюдать процесс десублимации в виде красивых рисунков на стеклах. Иней образуется похожим способом — резкое похолодание приводит к десублимации воздуха.
Влажность воздуха: испарение и конденсация
Такие процессы, как испарение и конденсация, становятся более логичными и простыми, если их рассмотреть на примере влажности воздуха.
Влажность воздуха говорит нам о том, сколько в воздухе содержится водяного пара. Любое количество пара в воздух не запихнешь, поэтому, во-первых, его там очень мало, а во-вторых, при избыточном количестве водяного пара происходит конденсация — это когда образуется роса.
Как влажность влияет на человека
Для человека влажность очень важна, потому что мы состоим из воды на 90%. Если окружающей среде нечего испарять, она будет испарять нас. Поэтому при низкой влажности мы чувствуем сухость во рту, а при высокой — волосы впитывают влагу, разбухают и начинают виться. На этом принципе построены некоторые гигрометры — приборы для измерения влажности. Они так и называются — волосяные гигрометры. Только внутри не человеческий волос, а конский, но принцип от этого не меняется.
При высокой влажности холод и тепло воспринимаются более чувствительно. Это связано с потливостью человека при высокой температуре. Такой механизм помогает нам бороться с жарой, но при высокой влажности пот не может испариться. При испарении пота мы теряем избыточное тепло, а в данном случае этого не происходит.
При низкой влажности происходит нечто похожее. Как ни странно, в мороз мы тоже потеем (намного меньше, но все-таки это происходит). Если влажность на улице низкая, то пот испарится из-под куртки и нам будет комфортно, а при высокой влажности — он там задержится и будет проводить тепло наружу, забирая у нас драгоценные Джоули тепла. Поэтому зимой в Петербурге холоднее, чем в Москве.
Влажностью можно управлять. Существуют мешочки с шариками адсорбентами, которые кладут в коробки с обувью, чтобы впитать лишнюю влагу. Чтобы окна не запотевали, можно насыпать в рамы соль, которая также впитает влагу. А если вам наоборот нужно больше влаги — берем увлажнитель воздуха (классная вещь!): он добавляет в воздух водяной пар.