расчет инсулина на еду при сахарном диабете 1 типа
Диа-арифметика сахарного диабета 1 типа (часть 1)
0.2 кг * Х кг веса = доза Лантуса (или Левемира) в сутки, вводимого вечером в 23.00.
Не надо создавать передозировку продлённого инсулина!
Углеводный коэффициент (УК). Сколько надо инсулина, чтобы усвоить 1 ХЕ еды. Считается по формуле: 12: (500 : СДИ) =Х (углеводный коэффициент)
ХЕ (хлебная единица). Надо бы было поставить этот показатель самым первым. Считается только для углеводов!
1 ХЕ = 12 гр. углеводов, все продукты можно измерить в этом показателе!
Таблицы с ХЕ людям с СД1 надо знать наизусть, как таблицу умножения. Тогда не придётся ограничивать себя в еде, вы сможете правильно ввести короткий инсулин на пищевую нагрузку.
Овощи тоже считаются, всеобщее заблуждение, что овощи можно не переводить в ХЕ. Потребность ХЕ в сутки: 1-3 года – 10-11 ХЕ\сутки, 4-11 лет – 16-17 ХЕ, 12-18 лет и взрослые – 19-21 ХЕ (макс 25 ХЕ).
ЦГ – целевая гликемия. Это индивидуальный показатель для каждого, то есть идеальные показатели сахара крови натощак и еду.
Обычно, натощак 5.0-7.0 ммоль/л – через 2 часа после еды – 5.0-7.8 ммоль/л.
АГ – актуальная гликемия. Это то, что СЕЙЧАС показал ваш глюкометр. Позже нам эти данные понадобятся.
СК – сахар крови. СК надо измерять натощак, после сна, перед чисткой зубов, перед основными приёмами пищи, перед сном, при ощущениях гипогликемии и гипергликемии.
СК утром 5.0-6.5 ммоль/л – значит дозы продленного и короткого инсулинов были вечером введены правильно, коррекция не нужна.
Если СК менее 5.0 ммоль/л более 3-5 дней подряд – это риск гипогликемии, надо снизить базу (Лантус или Левемир) накануне.
СК выше перед обедом – надо увеличить дозу короткого инсулина утром, СК выше перед ужином – увеличить дозу короткого инсулина перед обедом, выше перед сном – увеличить дозу короткого инсулина перед ужином.
Эти инсулины работают ещё 5 часов, это надо учитывать, считая инсулин на следующую еду!
Коррекция инсулина на ЕДУ. Формула такова:
(УК*ХЕ) +(АГ-ЦГ) : ФЧИ –АИ = Х единиц короткого инсулина на данную ЕДУ.
Коррекция высокого сахара.
(АГ-ЦГ): ФЧИ = Х единиц короткого инсулина для нормализации СК. В предыдущей формуле на еду – это всё учитывается!
Время экспозиции инулина. Время от начала введения инсулина до приёма пищи.
СК менее 5.0 ммоль/л – инсулин водится с едой, ниже 4.0 ммоль/л
(3.8 ммоль/л) – купирование гипогликемии, инсулин не вводить.
НЕ ленитесь рассчитать эти индексы для себя, в будущем будет проще!Всё будете делать уже автоматически. Каждый человек индивидуален. Эти расчеты – индивидуальный подход.
Во второй части мы продолжим считать ХЕ и инсулин на ЕДУ, физическую нагрузку разного типа, ОРВИ и т.д.
Расчет инсулина на еду при сахарном диабете 1 типа
Регистратура: (0152) 44 72 00,
Адрес: 230030, г.Гродно, ул. Болдина, 11
Полная информация и схема проезда



Коррекция дозы инсулина в зависимости от количества углеводных единиц, физической нагрузки, различных физиологических состояний, при острых заболеваниях, сопутствующей патологии и т.д. Особенности проведения самоконтроля гликемии в вышеуказанных случаях.
«Корригирующая» доза(КД)
При гликемии перед едой, превышающей целевую, к рассчитанной выше дозе добавляется «корригирующая» доза (КД) для понижения гликемии. Для этого необходимо выяснить индивидуальную чувствительность к инсулину (ЧИ), для чего используется формула:
Таким образом, если у больного гликемия 14 ммоль/л (уровень целевой гликемии 8 ммоль/л), с учетом ЧИ величина коррекционной дозы (КД) составит (14 – 8) / 4,1= 1,5. Следовательно, на съеденные 4 ХЕ к расчетным 3 Ед. добавляется еще 1,5 ЕД. Всего, выходит,4,5 ЕД инсулина короткого действия.
Таким образом, система ХЕ как метод подсчета потребляемых углеводов используется у пациентов с СД 1-го типа не с целью ограничения потребления углеводов, а в связи с необходимостью соотносить его с дозами инсулина.
Примеры коррекции доз короткого инсулина (по гликемии перед едой)
Перед приемом пищи уровень сахара в норме. В этом случае вторая составляющая КД (на высокий сахар) будет равна нулю, а величина (УК)первой будет зависеть от количества ХЕ, которые вы употребите в данный прием пищи.
Перед приемом пищи сахар крови повышен (11,4 ммоль/л). В этом случае мы делаем дозу, состоящую из двух компонентов: на снижение высокого сахара и на усвоение углеводов.
Поводом для уменьшения плановой дозы инсулина служит снижение уровня глюкозы до 3,3-3,9 ммоль/л или возникновение гипогликемии.
Рекомендации по коррекции доз инсулина
Устойчивые изменения уровня глюкозы крови в определенное время суток, выявленные по записям в дневнике, могут служить основанием для коррекции доз инсулина и схемы инсулинотерапии. Чтобы убедиться, хватает ли инсулина на еду (болюса), необходимо проверить сахар крови перед едой и через 2–2,5 часа после — колебание гликемии не должны превышать 1,5–2 ммоль/л.
Устойчивые изменения уровня глюкозы крови в определенное время суток
Если уровень глюкозы крови после завтрака обнаруживает тенденцию к повышению, можно несколько увеличить дозу инсулина короткого действия, вводимую перед завтраком.
Наоборот, если уровень глюкозы в интервале между завтраком и обедом снизился и, особенно, если в это время появляются признаки гипогликемии, следует снизить утреннюю дозу инсулина короткого действия.
Подбор вечерней дозы NРH-инсулина
Если возникают ночные гипогликемии, когда в промежутке между 0 и 3 часами ночи уровень базального инсулина выше, чем обычная потребность в нем, то уменьшение дозы пролонгированного инсулина, вводимого перед сном, снижает вероятность возникновения ночной гипогликемии, однако часто приводит к утренней гипергликемии.
Это, в свою очередь, связано с тем, что в ранние утренние часы физиологическая потребность в инсулине резко возрастает («феномен утренней зари»). Нивелировать повышение гликемии в утренние часы можно за счет дополнительного введения короткого или ультракороткого инсулина в 4–5 часов утра.
ГИПЕРГЛИКЕМИЯ НАТОЩАК
Что делать, если у тебя высокий уровень сахара в крови утром натощак, и почему так происходит?
Прежде всего надо найти причину :
1.Недостаточная доза продленного инсулина получена вечером накануне (смотрите по сахару крови среди ночи — гликемия не должна превышать целевую 6–9 ммоль/л).
2.Ночная гипогликемия (проверить сахар в крови в 2 часа ночи).
Доза инсулина продленного действия относительно постоянна. Она подбирается так, чтобы инсулин между приемами пищи удерживал гликемию от повышения и не снижал ее. Эта доза периодически пересматривается на основании данных дневника самоконтроля
Примеры коррекции доз инсулина (сопутствующее заболевание)
Если у больного гипертермия, то дозировка инсулина перед едой должна складываться из двух составляющих: на высокую температуру (10% от суточной дозы короткого инсулина) и на ХЕ, которые вы съедите.
Если перед приемом пищи сахар крови очень высокий и даже есть ацетон, то дозировка инсулина должна складываться из: дозы на погашение сахара (20% от суточной дозы инсулина короткого действия) и на ХЕ, которые вы съедите (вторая составляющая может быть равна нулю).
Основные принципы инсулинотерапии:
Осложнения инсулинотерапии Гипогликемия
Особенно велик риск тяжелой гипогликемии (судорог или комы) у детей младшего возраста, поскольку они неспособны распознать предвестники гипогликемии.
Самая частая причина гипогликемии — передозировка инсулина.
Больные, живущие в тяжелых семейных условиях, и больные в тяжелой депрессии (особенно подростки) могут намеренно вводить чрезмерные дозы инсулина.
Постинъекционные липодистрофии
Часто в местах инъекций инсулина развивается липогипертрофия, обусловленная усилением образования жировой ткани. Липогипертрофия нарушает всасывание инсулина.
Профилактика липодистрофии: частая смена мест инъекций, массаж, физиотерапия
Аллергия к инсулину
Через несколько минут или часов после инъекции инсулина могут наблюдаться местные аллергические реакции (краснота, зуд, отек, уплотнение, ощущение жара).
В редких случаях возможны общие аллергические реакции: крапивница или отек.
Синдром передозировки инсулина
В таких случаях гипергликемию можно предупредить, снижая дозы инсулина.
Расчет инсулина на еду при сахарном диабете 1 типа
Регистратура: (0152) 44 72 00,
Адрес: 230030, г.Гродно, ул. Болдина, 11
Полная информация и схема проезда



Инсулинотерапия: виды инсулина, схемы инсулинотерапии, правила расчета дозы инсулина.
Определение
Сахарный диабет 1-го типа – это заболевание, обусловленное недостатком инсулина. Инсулин – гормон, который вырабатывается в бета- клетках островков поджелудочной железы. Единственный гормон, снижающий уровень глюкозы в крови!
При сахарном диабете 1-го типа единственный и основной метод лечения – введение инсулина, который восполняет дефицит инсулина.
Взаимодействие инсулина и глюкозы в норме
Для поступления глюкозы в клетку (мышечную, жировую, печеночную) необходим инсулин. Он, как ключ, открывает клетку для глюкозы. Если инсулина нет – клетка останется «голодной».
Виды инсулинов
В применяются только человеческие генноинженерные инсулины и инсулиновые аналоги.
Препараты инсулина короткого действия – пищевые
Препараты инсулина короткого действия
Аналоги человеческого инсулина ультракороткого действия
Препараты инсулина продленного действия (фоновые)
Аналог человеческого инсулина продленного действия
Физиологическая секреция инсулина в норме
Также в ответ на прием пищи происходит выброс дополнительной порции инсулина, чтобы поддержать уровень гликемии в пределах нормы во время приема пищи и после него, что носит название «пищевой секреции». При физической нагрузке потребность в инсулине снижается.
Нормальная секреция инсулина у здоровых людей
Цель заместительной терапии инсулином- добиться нормальных показателей гликемии за счет максимально физиологичного введения инсулина, поддержание состояния углеводного обмена близкого к тому, которое имеется у здорового человека.
На сегодняшний день наиболее физиологичной является интенсивная схема введения инсулина. Интенсивная схема инсулинотерапии – многократное введение инсулина и постоянный контроль уровня гликемии с самостоятельной коррекцией доз вводимого инсулина с учетом уровня гликемии, количества углеводов, физической нагрузки.
Интенсивная схема инсулинотерапии
Интенсифицированная инсулинотерапия с использованием двух инъекций инсулина средней продолжительности действия
Интенсифицированная инсулинотерапия с использованием одной инъекции аналога инсулина длительного действия
«Углеводный коофициент»(УК)
Это количество короткого инсулина вводимого перед едой на 1 ХЕ.
(УК)= равен соотношению дозы короткого инсулина в ЕД за сутки и количества углеводов, принятых с пищей в ХЕ за сутки.,
Этот метод приблизительный, и показатель УК перепроверяется и уточняется в течение первых двух суток в результате постоянного гликемического контроля.
Но это условие выполняется, если уровень гликемии не выше целевого (от6 до 8 ммоль/л).
Современная инсулинотерапия сахарного диабета 1 типа у детей и подростков
Сахарный диабет 1 типа (СД 1 типа), называвшийся до недавнего времени инсулинозависимым, а еще раньше — ювенильным сахарным диабетом, поражает в основном людей молодого возраста и детей. В последние годы наблюдается
Сахарный диабет 1 типа (СД 1 типа), называвшийся до недавнего времени инсулинозависимым, а еще раньше — ювенильным сахарным диабетом, поражает в основном людей молодого возраста и детей. В последние годы наблюдается всплеск заболеваемости сахарным диабетом 1 типа, наиболее выраженный у детей и подростков. За 25 лет заболеваемость СД 1 типа среди детей московской популяции выросла в два раза. В настоящее время в Москве насчитывается около 1200 детей с СД в возрасте до 15 лет.
СД 1 типа относится к аутоиммунным заболеваниям, при которых в результате процессов аутоагрессии против β-клеток островков поджелудочной железы происходит их разрушение. После гибели более 85% β-клеток развивается абсолютная инсулиновая недостаточность, в результате которой появляются гипергликемия и другие метаболические нарушения. С начала промышленного выпуска препаратов инсулина после успешных опытов Бантинга и Беста на панкреатэктомированных собаках и по настоящее время инсулин — основное и единственное средство лечения СД 1 типа. Прошло более 80 лет с начала клинического применения инсулина. Инсулинотерапия за это время претерпела большие изменения, связанные с улучшением качества инсулина и совершенствованием схем введения препарата.
Лечение СД 1 типа состоит из нескольких компонентов:
Основная цель современной инсулинотерапии — поддержание состояния углеводного обмена, близкого к тому, которое имеется у здорового человека. Постоянная гипергликемия вызывает развитие и прогрессирование специфических осложнений: диабетической нефро-, ретино- и нейропатии, что приводит к повышенной инвалидизации и преждевременной смертности пациентов. В связи с этим, учитывая важную роль адекватной инсулинотерапии в профилактике сосудистых осложнений, при разработке новых препаратов и схем лечения СД необходимо стремиться к сохранению углеводного обмена и поддержанию его в пределах показателей, соответствующих нормальным, в течение длительного времени.
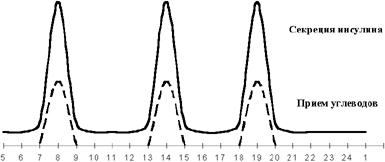 |
| Рисунок 1. Физиологическая секреция инсулина в норме. |
В физиологических условиях секреция инсулина происходит в два этапа (см. рисунок 1): поджелудочная железа секретирует инсулин постоянно (базальная инсулинемия), а в ответ на соответствующие стимулы (посталиментарная гипергликемия, или гипергликемия, вызванная действием контринсулярных гормонов) повышает секрецию инсулина. При этом нормогликемия в здоровом организме обеспечивается быстрой адекватной секрецией инсулина, а также коротким периодом полужизни (около 4 мин) циркулирующего в крови инсулина. Печень принимает активное участие в поддержании гомеостаза глюкозы, депонируя ее в виде гликогена после еды и выделяя вновь в кровь из депо путем активизации процесса гликогенолиза в перерывах между приемами пищи. При этом очень важно, что инсулин из поджелудочной железы поступает в систему воротной вены и далее — в печень — главный орган-мишень, где он наполовину инактивируется, участвуя в превращении глюкозы в гликоген. Остающиеся 50% инсулина через большой круг кровообращения попадают к периферическим органам и тканям. Именно более высокий уровень инсулина в портальной системе, по сравнению с периферической циркуляцией, обеспечивает активное депонирование глюкозы в печени на фоне других инсулинзависимых органов.
У больных диабетом введенный экзогенный инсулин из подкожного депо медленно всасывается в общий кровоток, где концентрация его длительно остается нефизиологично высокой. В результате у пациентов с сахарным диабетом наблюдаются более высокая, чем у здоровых, посталиментарная гипергликемия и склонность к гипогликемии в более поздние часы. Поэтому больные сахарным диабетом должны приспосабливать свой режим жизни к профилю действия вводимого инсулина. Неизбежное возникновение стрессовых ситуаций требует дополнительной коррекции дозы экзогенного инсулина. Кроме того, из общего кровотока инсулин одновременно поступает в печень и другие органы-мишени. В результате гликоген депонируется в первую очередь в мышечной ткани, а запасы в печени его постепенно снижаются. Это является одной из причин развития гипогликемий, так как мышечный гликоген не участвует в поддержании нормогликемии. Добиться физиологического соотношения концентрации гормона в портальной системе и на периферии при современных методах введения экзогенного инсулина невозможно, и это одна из наиболее сложных проблем заместительной инсулинотерапии.
Тем не менее с совершенствованием методов инсулинотерапии появилась возможность максимально приблизить показатели углеводного обмена к таковым у здоровых людей у ряда больных СД 1 типа. И процент таких больных постепенно увеличивается по мере совершенствования методов компенсации заболевания. В последнее время убедительно доказано, что только хорошая компенсация сахарного диабета может служить надежным средством профилактики специфических осложнений. В связи с этим Всемирной организацией здравоохранения были разработаны новые целевые уровни показателей углеводного обмена, к которым врачи-практики вместе со своими больными должны стремиться. Оценка степени компенсации СД 1 типа основывается на клинических (нормальное физическое и половое развитие, отсутствие осложнений) и лабораторных показателях углеводного (гликемия, глюкозурия, гликированный гемоглобин) и жирового (холестерин, триглицериды, липопротеины) обмена. Соглашение по основным принципам лечения детей и подростков с СД 1 типа (ISPAD Consensus for the Management of Type 1 Diabetes Mellitus in Children and Adolescens, 2000) рекомендует следующие критерии эффективности инсулинотерапии:
У детей в возрасте до шести лет с учетом отрицательного влияния гипогликемий на развитие мозга эти показатели должны быть на верхней границе или несколько выше. В отношении гликированного гемоглобина рекомендуется, чтобы концентрация его была приближена к норме насколько это возможно, однако риск развития тяжелых гипогликемий при этом должен быть сведен к абсолютному минимуму.
Инсулины, применяемые в детской практике
Современные препараты инсулина в зависимости от происхождения разделяют на две группы — животные и человеческие (полусинтетический и биосинтетический инсулины). На протяжении 80 лет для лечения СД применяли говяжий и свиной инсулины, которые по составу отличаются от человеческого на три и одну аминокислоты соответственно. При этом иммуногенность максимально выражена у говяжьих инсулинов, минимальная, естественно, — у человеческих. Человеческие инсулины стали применяться два последних десятилетия и буквально произвели революцию в методах лечения больных диабетом.
При получении человеческого инсулина полусинтетическим методом производится замена аминокислоты аланина в 30-й позиции В-цепи свиного инсулина на треонин, находящийся в этом положении в человеческом инсулине. В полусинтетическом инсулине присутствуют в небольшом количестве примеси соматостатина, глюкагона, панкреатических полипептидов, имевшиеся в свином инсулине, который является субстратом для производства данного вида человеческого инсулина. Биосинтетический инсулин не имеет этих примесей и обладает меньшей иммуногенностью. При его производстве в клетку пекарских дрожжей или E.coli генно-инженерным способом вводится рекомбинантная ДНК, содержащая ген человеческого инсулина. В результате дрожжи либо бактерии начинают синтезировать человеческий инсулин. Человеческие генно-инженерные инсулины представляют собой более прогрессивную форму и должны рассматриваться как препараты первого ряда при выборе способа лечения. В России у детей и подростков в последние годы рекомендованы к применению только человеческие генно-инженерные инсулины.
Современные генно-инженерные инсулины различаются по длительности действия:
Их фармакокинетические характеристики представлены в таблице 1.
Последнее десятилетие открыло новую эру в инсулинотерапии: речь идет о получении аналогов человеческих инсулинов с новыми фармакокинетическими свойствами. К ним относятся инсулины ультракороткого действия (хумалог и новоРапид) и продленные беспиковые аналоги человеческого инсулина (детемир и лантус).
Особое место в лечении сахарного диабета в детском и подростковом возрасте занимают инсулины ультракороткого действия — хумалог и новоРапид. Получают беспиковые аналоги инсулина путем замены аминокислот, отвечающих за процессы самоассоциации молекул инсулина, что приводит к ускорению процессов их всасывания из подкожного депо. Так, хумалог был получен путем взаимного изменения положения аминокислот пролин и лизин в 28-й и 29-й положениях в В-цепи, новоРапид — путем замены аминокислоты пролин в том же 28-м положении на аспарагин. Это не изменило биологической активности инсулинов, но привело к полезному изменению его фармакокинетических свойств. При подкожном введении хумалог и новоРапид имеют более быстрое начало и пик действия, параллельные уровню посталиментарной гипергликемии, и меньшую продолжительность, что дает возможность вводить эти препараты непосредственно перед приемом пищи, избегая (при желании) частых перекусов. При использовании аналогов человеческих инсулинов повышаются возможности в компенсации углеводного обмена, что выражается в уменьшении показателей гликированного гемоглобина, и снижается частота тяжелых гипогликемий.
Самым последним достижением в области инсулинотерапии стало введение в клиническую практику инсулина лантус, который является первым беспиковым аналогом человеческого инсулина 24-часового действия. Получен путем замены аминокислоты аспарагин на глицин в 21-м положении А-цепи и добавления двух аминокислот аргинина к концевой аминокислоте в Б-цепи. Результатом явилось изменение рН раствора инсулина после введения его в подкожно-жировую клетчатку с 4,0 до 7,4, что вызывает образование микропреципитатов, замедляющих скорость всасывания инсулина и обеспечивающих его постоянный и стабильный уровень в крови в течение 24 ч.
Лантус может вводиться в любое время суток, у подростков — предпочтительнее в вечерние часы. Начальная его доза составляет 80% от суммарной суточной дозы пролонгированного инсулина. Дальнейшая титровка дозы проводится по показателям сахара крови натощак и в ночные часы. Уровень гликемии после завтрака, в дневные и вечерние часы регулируется инсулином короткого или ультракороткого действия. Назначение лантуса позволяет избежать дополнительных инъекций короткого инсулина в ранние утренние часы у большинства подростков с феноменом «утренней зари», вызывает достоверное снижение утренней гликемии, а также уменьшает лабильность углеводного обмена у многих больных.
Инсулин детемир также является беспиковым аналогом продленного действия, пролонгирующий эффект которого был достигнут благодаря присоединению цепочки из 14 остатков жирных кислот в 29-й позиции В-цепи. Детемир вводится дважды в сутки.
В состав смешанных инсулинов входит инсулин средней продолжительности и короткого действия в различных соотношениях — от 90 к 10 до 50 к 50. Смешанные инсулины более удобны, поскольку их применение позволяет уменьшить количество инъекций, проводимых с помощью шприц-ручек. Однако в детской практике они не нашли широкого применения в связи с необходимостью у многих больных достаточно часто изменять дозу короткого инсулина в зависимости от показателей гликемии. Тем не менее при стабильном течении сахарного диабета (особенно в первые годы заболевания) с помощью смешанного инсулина возможно достижение хорошей компенсации.
Режимы инсулинотерапии
Имеющиеся общие рекомендации по режиму инсулинотерапии являются только основой для разработки индивидуального режима, который должен учитывать физиологические потребности и сложившийся образ жизни каждого ребенка.
Наибольшее распространение в настоящее время получила интенсифицированная (или базисно-болюсная) схема, которая заключается во введении короткого инсулина перед каждым основным приемом пищи и пролонгированного инсулина от одного до трех раз в сутки (см. рисунок 2). Наиболее часто пролонгированный инсулин вводится дважды — в вечерние и утренние часы. При этом предпринимаются попытки имитировать с помощью продленного инсулина базальную секрецию, а с помощью инсулина короткого действия посталиментарную секрецию.
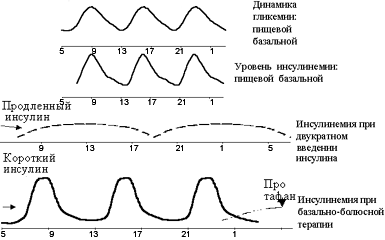 |
| Рисунок 2. Графическое обоснование базисно-болюсного принципа инсулинотерапии. |
Введение третьей инъекции пролонгированного инсулина получило название оптимизации базальной инсулинотерапии. Вопрос о необходимости и времени введения третьей инъекции решается на основании показаний гликемического профиля. Если гликемия повышается перед ужином при ее нормальных показателях через 1,5-2 ч после обеда, вводится дополнительная инъекция продленного инсулина перед обедом (см. рисунки 3, 4). Как правило, такая ситуация возникает при позднем (в 19.00-20.00) ужине. При раннем ужине (в 18.00) и введении второй инъекции пролонгированного инсулина перед сном гипергликемия нередко наблюдается в 23.00. В этой ситуации хороший эффект дает назначение дополнительной инъекции продленного инсулина перед ужином.
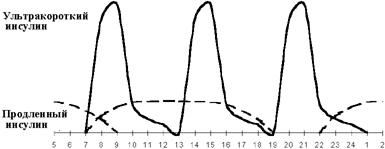 |
| Рисунок 3. Интенсифицированная инсулинотерапия. |
Такая схема позволяет в какой-то степени приблизиться к физиологической секреции инсулина у здоровых людей. Кроме того, она дает возможность расширить режим жизни и питания больного сахарным диабетом. Психологическим недостатком ее является необходимость частых инъекций и частого контроля гликемии, однако это нивелируется в настоящее время благодаря современным технологическим достижениям (удобные шприц-ручки с атравматичными иглами и глюкометры с автоматами для безболезненного прокалывания пальца). Учащение эпизодов гипогликемических реакций, которое вменяют иногда «в вину» интенсифицированной инсулинотерапии, является не столько следствием применяемой схемы, сколько результатом стремления врачей достичь нормогликемии. При решении данного вопроса всегда следует искать компромисс, стремясь поддержать тот минимальный уровень гликемии, который не вызывает частых гипогликемических реакций. Этот уровень гликемии для каждого ребенка достаточно индивидуален.
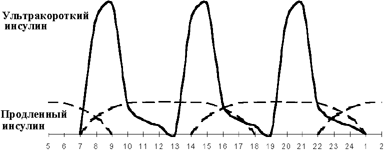 |
| Рисунок 4. Оптимизация интенсифицированной инсулинотерапии. |
У детей первых двух лет жизни интенсифицированная схема применяется реже.
Традиционная схема инсулинотерапии заключается во введении инсулина короткого и пролонгированного действия два раза в сутки — перед завтраком и ужином. Применение ее возможно у ряда детей в первые один-два года заболевания, редко при большей длительности сахарного диабета (см. рисунок 5).
 |
| Рисунок 5. Традиционная схема инсулинотерапии. |
Если небольшая доза короткого инсулина вводится перед обедом, такая схема может быть искусственно продлена на некоторое время путем увеличения дозы продленного инсулина перед завтраком и небольшого перераспределения в питании (перенос одной-двух хлебных единиц с обеда на второй завтрак).
 |
| Рисунок 6. Нетрадиционные схемы инсулинотерапии. |
Кроме того, существует ряд нетрадиционных схем (см. рисунок 6):
Эти схемы иногда используются у больных с небольшим сроком заболевания сахарным диабетом при частичной сохранности функции β-клеток.
В любом случае выбор схемы инсулинотерапии определяется не столько желанием врача или семьи больного, сколько оптимальным профилем введения инсулина, который обеспечивает компенсацию углеводного обмена.
Доза инсулина
В детском возрасте потребность в инсулине, рассчитанная на 1 кг веса, нередко выше, чем у взрослых, что обусловлено большей скоростью аутоиммунных процессов, а также активным ростом ребенка и высоким уровнем контринсулярных гормонов в период полового созревания. Доза инсулина изменяется в зависимости от возраста и длительности заболевания.
В первые один-два года с момента начала заболевания потребность в инсулине составляет в среднем 0,5-0,6 ЕД/кг массы тела. В 40–50% в первые месяцы наблюдается частичная ремиссия заболевания, когда после достижения компенсации углеводного обмена потребность в инсулине снижается до минимальной — 0,1-0,2 ЕД/кг массы, а у некоторых детей даже при полной отмене инсулина при соблюдении диеты удается поддерживать нормогликемию. (Наступление ремиссии тем более вероятно, чем раньше установлен диагноз диабета и начата инсулинотерапия, чем выше качество вводимого инсулина и чем лучшей компенсации углеводного обмена удается достичь.)
Через пять лет от момента заболевания диабетом у большинства больных β-клетки полностью прекращают функционировать. При этом потребность в инсулине обычно повышается до 1 ЕД/кг массы. В период полового созревания она вырастает еще больше, достигая у многих подростков 1,5, иногда 2 ЕД/кг. В последующем доза инсулина снижается в среднем до 1 ЕД/кг. После длительной декомпенсации сахарного диабета потребность в инсулине может достигать 2-2,5, иногда 3 ЕД/кг с последующем снижением дозы, в отдельных случаях вплоть до исходной.
Соотношение пролонгированного и короткого инсулина сдвигается: от преобладания пролонгированного инсулина у детей первых лет жизни к преобладанию короткого инсулина у подростков (см. таблицу 2).
Как и у взрослых, у детей на одну хлебную единицу в утренние часы требуется несколько больше инсулина, чем в обед и в ужин.
Следует подчеркнуть, что это лишь общие закономерности, у каждого ребенка потребность в инсулине и соотношение инсулинов различной длительности имеют свои индивидуальные особенности.
Осложнения инсулинотерапии
Перспективы совершенствования инсулинотерапии в России
Внедрение аналогов человеческих инсулинов расширяет возможности достижения компенсации, улучшения течения заболевания у детей и подростков с сахарным диабетом.
Инсулиновые помпы, в течение ряда лет применяемые за рубежом, сегодня появились и на отечественном рынке, однако применение их ограничено из-за высокой стоимости.
В настоящее время за рубежом ведутся исследования, посвященные эффективности и безопасности применения ингаляционных видов инсулина, с которыми связана надежда на возможность отказа от постоянных введений короткого инсулина перед приемами пищи.
Вопрос о клиническом использовании трансплантации островковых клеток останется открытым до тех пор, пока не будут найдены средства защиты пересаженных клеток от того же аутоиммунного процесса, который поражает собственные β-клетки. В настоящее время трансплантация β-клеток за рубежом осуществляется только у больных с развившейся хронической почечной недостаточностью, одновременно с трансплантацией почки и назначением иммунодепрессантов. Все остальные работы по трансплантации носят исследовательский характер и производятся на добровольцах. Однако канадским исследователям удалось получить первые обнадеживающие результаты.
В. А. Петеркова, доктор медицинских наук, профессор
Т. Л. Кураева, доктор медицинских наук
Е. В. Титович, кандидат медицинских наук
Институт детской эндокринологии ГУ ЭНЦ РАМН, Москва
















