каждой белковой молекуле соответствует что
Генетический код. Биосинтез белка
теория по биологии 🌿 основы генетики
Генетическая информация и генетический код
Каждый вид имеет свой собственный, отличный от других видов, набор белков. Интересно то, что белки, выполняющие идентичные функции у разных видов могут быть похожими или даже абсолютно идентичными.
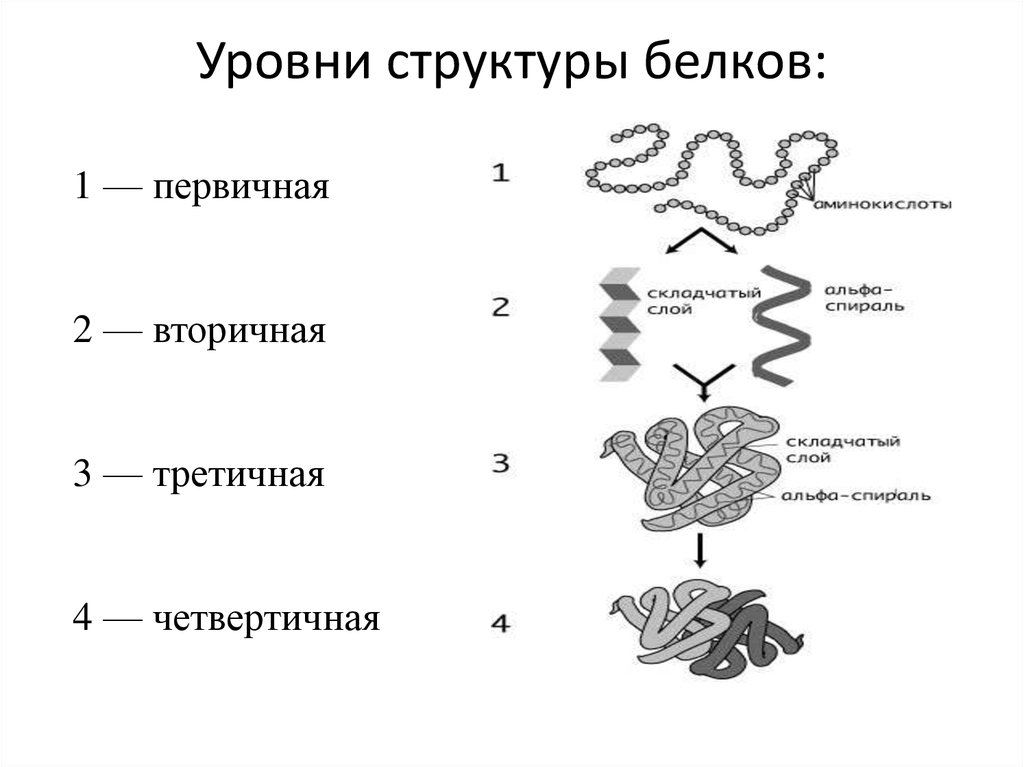
У белков есть несколько состояний их структур:
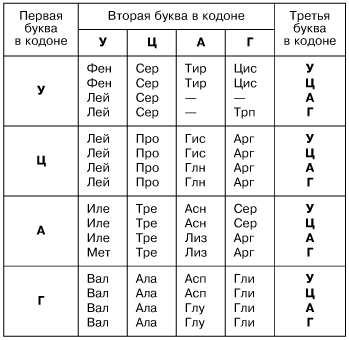
Именно первичная структура является определяющей свойства белка. Эта структура – цепь из аминокислот. Аминокислоты, в свою очередь, представляют собой ряд триплетов из нуклеотидов. Решая генетические задачи, обращаются как раз-таки к знакомой таблице:
Каждая аминокислота кодируется тремя нуклеотидами, которые составляют триплет или иначе кодон. Именно последовательность нуклеотидов называется генетической информацией, а участок последовательности, в котором хранится информация о первичной структуре белка это и есть ген.
Нуклеотиды, составляющие ДНК и РНК различаются:
В состав ДНК входят:
В состав РНК входят:
Кроме того, в составе РНК (рибонуклеиновой кислоты) сахар рибоза, а ДНК (дезоксирибонуклеиновой кислоты) — дезоксирибоза. РНК — одноцепочечная, а ДНК — двухцепочечная.
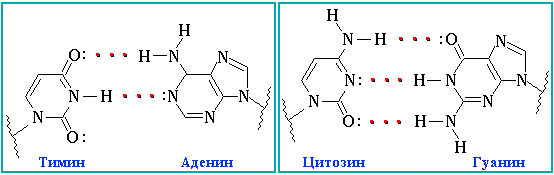
Между нуклеотидами есть водородные связи. Они могут быть как двойные, так и тройные. Нуклеотиды не могу быть связаны в случайном порядке. Для этого существует принцип комплементарности ДНК, по которому аденин одной цепи ДНК соединяется с тимином другой цепи ДНК, другая пара в ДНК – гуанин – цитозин. В РНК все аналогично, за исключением того, что вместо тимина там урацил. Между парами А-Т/А-У – две водородных связи, а между парами Ц-Г – три. На письме это обозначается чёрточками: двойная связь как знак «равно», а тройная – три горизонтальные черты.
Свойства генетического кода
Транскрипция и трансляция
Из цитологии известно, что генетическая информация у эукариотических клеток заключена в ядре в виде ДНК. Однако процесс биосинтеза белка происходит в цитоплазме на рибосомах.
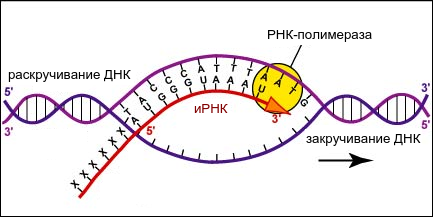
Спиральная цепь ДНК при раскручивается, в это время по одной из цепочек ДНК строится комплементарная цепь. Из ядра в цитоплазму информация выходит в виде информационной РНК (иРНК). иРНК комплементарная одной из цепей ДНК. Этот процесс переписывания называется транскрипцией. Полученная цепь практически идентичная другой цепи ДНК, за исключением того, что вместо тимина там урацил.В процессе участвует специальный фермент РНК-полимераза.
Теперь в ядре есть цепочка, которая уже начала процесс биосинтеза. Как говорилось выше, процесс ассимиляции идет на рибосомах. иРНК выходит в цитоплазму через поры ядерной мембраны
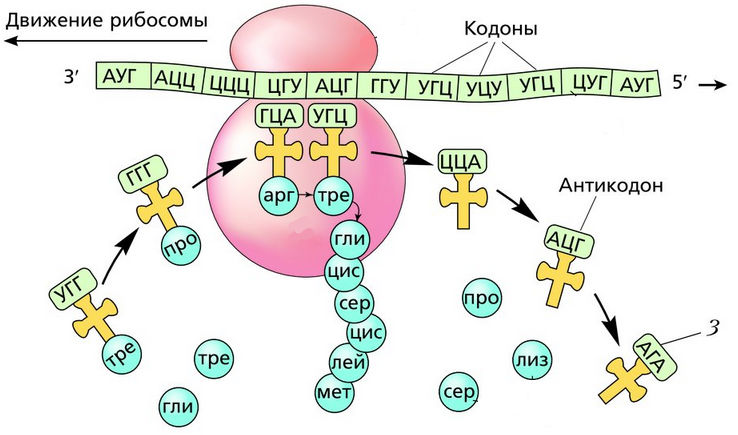
тРНК по форме напоминает лист клевера, а по принципу работы – штамп. На него, прямо как чернила, наслаиваются кодоны.
В цитоплазме начинается процесс трансляции, то есть перевод последовательности нуклеотидов информационной РНК в последовательность аминокислот белка.
Рибосома захватывает стартовый конец цепи иРНК. Затем она начинает двигаться по цепи, одна остановка рибосомы происходит на 6-ти нуклеотидах. В это время молекула тРНК, на которых есть триплет аминокислоты «подлетает» к цепи, в месте, где находится рибосома. За время остановки рибосомы транспортная РНК успевает распознать свою пару на цепи иРНК, которая называется антикодоном. Тогда тРНК «ставит свой штамп», оставляя на цепи свой кодон. Между нуклеотидами образуются водородные связи. Так нарастает новая цепь. На одной информационной РНК работает сразу много рибосом, поэтому работа идет очень быстро. Совокупность рибосом, синтезирующих на одной иРНК, называется полисомой.
По окончанию процесса биосинтеза, цепочка отсоединяется от рибосомы и принимает свою природную структуру: вторичную, третичную или четвертичную.
pазбирался: Надежда | обсудить разбор | оценить
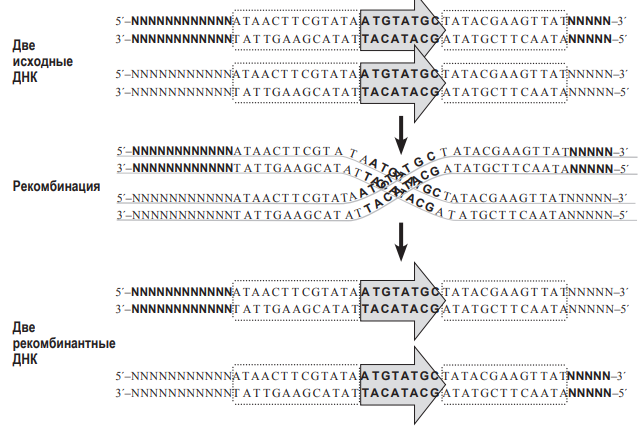
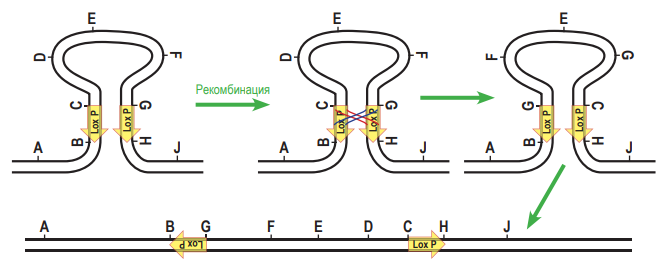
В современной генетической инженерии часто применняют технологии, связанные с гомологичной рекомбинацией ДНК непосредственно в живом объекте. Один из примеров – система CRE-Lox P. Lox P – это последовательность нуклеотидов в ДНК фага Р1. Она состоит из 34 нуклеотидов. В середине располагается несимметричная последовательность из 8 нуклеотидов (показана серой стрелкой на рисунке). По краям располагаются так называемые палиндромные последовательности из 13 нуклеотидов (выделены на рисунке как пунктирные блоки). Они симметричны (чтобы в этом убедиться, достаточно прочитать обе последовательность от 5´- конца к 3´- концу). Именно эти палиндромные участки узнаёт особый фермент, вызывающий рекомбинацию, который обозначают CRE. Будем в дальнейшем называть этот фермент рекомбиназой CRE. Для того, чтобы состоялась рекомбинация, два сайта Lox P должны расположиться параллельно друг другу. Рекомбиназа CRE узнает эти сайты, внесет в ДНК разрезы в определённых местах, а затем 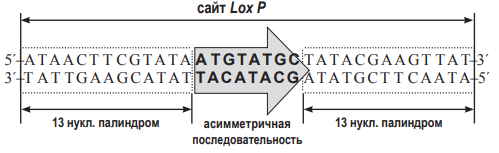

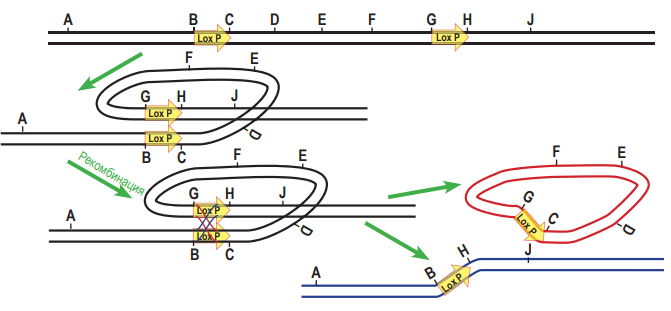
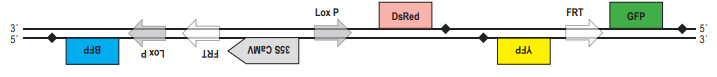
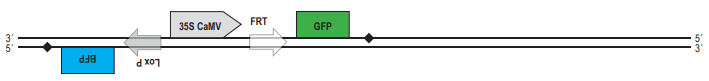
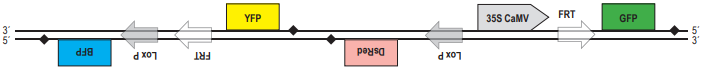
pазбирался: Надежда | обсудить разбор | оценить
pазбирался: Надежда | обсудить разбор | оценить
Сначала найдём место расщепления плазмиды рестриктазой BglII: 


pазбирался: Надежда | обсудить разбор | оценить
По принципу комплементарности строим
Самостоятельная работа «Белки: строение и функции»
Самостоятельная работа «Белки: строение и функции»
1. Аминокислоты отличаются друг от друга:

в) карбоксильной группой;
г) химическим составом.
2. Определите, что изображено на рисунке:
3. Для большинства белков характерна структура пространственной организации молекулы:
4. Одна из важнейших функций белков:
5. Все белки состоят из:
б) нуклеиновых кислот;
6. Молекулы белков отличаются друг от друга:
а) последовательностью чередования аминокислот;
б) количеством аминокислот в молекуле;
в) формой третичной структуры;
г) всеми указанными особенностями.
7. К какой структуре белка относится глобула?
8. Денатурация – это:
а) регулирование физиологическими процессами организма;
б) утрата белковой молекулой своей структуры;
в) предохранение организма от чужеродных белков.
9. При понижении температуры активность ферментов:
б) периодически изменяется;
10. В каком из указанных процессов белки НЕ участвуют?
б) транспорт веществ;
в) кодирование наследственной информации.
11. Установите соответствие между протеидом и его особенностью:
1) нуклеопротеид а) содержит небелковый компонент – липид;
2) гликопротеид б) содержит небелковый компонент – углевод;
3) металлопротеид в) содержит небелковый компонент – атом металла;
4) липопротеид г) содержит небелковый компонент – НК.
Самостоятельная работа «Белки: строение и функции»
1. Белки живых организмов составляют:
2. Денатурация белка:
а) всегда обратима, так как белок легко восстанавливает свою естественную структуру;
б) редкий процесс, так как связи, формирующие пространственные структуры белка, очень прочные;
в) лежит в основе ферментативной функции белков;
г) не затрагивает первичную структуру.
3. Примером запасающей функции белков является:
а) накопление белков в семенах бобовых;
б) наличие белков в мембранах клеток;
в) участие белков в иммунном ответе организма;
г) возможность гемоглобина образовывать непрочные соединения с кислородом и углекислым газом.
4. Среди органических веществ первое место, как по количеству, так и по значению занимают:
г) нуклеиновые кислоты.
5. Вторичная структура белка поддерживается:
а) пептидными связями;
б) водородными связями;
в) дисульфидными связями;
г) всеми перечисленными видами связи.
6. Аминокислоты в молекуле белка соединены посредством:
в) водородной связи;
г) связи между радикалами кислот.
7. Цепочка из аминокислот, соединённых пептидной связью, обладает структурой:
8. Последовательность аминокислот в молекуле белка зависит от:
в) их случайного сочетания.
9. В защите организма от кровопотерь участвует:
10. Выбери функции характерные для белков:
а) каталитическая, защитная, транспортная;
б) кроветворная, рефлекторная;
11. Установите соответствие между структурной организацией белка и ее изображением:

Самостоятельная работа «Белки: строение и функции»
Какие соединения являются мономерами молекул белка?
Какая часть молекул аминокислот отличает их друг от друга?
Сколько из известных аминокислот участвуют в синтезе белков?
Посредством какой химической связи соединены между собой аминокислоты в молекуле белка первичной структуры?
В каких органеллах клетки синтезируются белки?
Какие структуры молекул белка способны нарушаться при денатурации, а затем вновь восстанавливаться?
Сколько энергии освобождается при расщеплении 1г белка?
Посредством какой химической связи поддерживается вторичная структура белковой молекулы?
Сколько известно незаменимых аминокислот?
Какие аминокислоты организм получает в готовом виде вместе с пищей?
Какие аминокислоты, синтезируются в организме?
Мономер белковой молекулы
Структура белковой молекулы, возникающая в результате соединения нескольких глобул в сложный комплекс.
Структура белковой молекулы, представляющая линейную последовательность аминокислот, в составе полипептидной цепи.
Белки, состоящие только из аминокислот.
Структура белка, возникающая в результате образования водородных связей между СО– и NН–группами разных аминокислотных остатков полипептидной цепи.
Белки, содержащие небелковую часть.
Утрата белковой молекулой природной структуры, под воздействием температуры, химических веществ, обезвоживания, облучения и других факторов.
Белки, содержащие в себе углеводы, жиры, нуклеиновые кислоты.
Белок, состоящий только из белковых молекул.
Изменяемой частью аминокислоты является.
Восстановление утраченных структур.
Самостоятельная работа «Белки: строение и функции»
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
Курс профессиональной переподготовки
Методическая работа в онлайн-образовании
Курс повышения квалификации
Современные педтехнологии в деятельности учителя
Ищем педагогов в команду «Инфоурок»
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
также Вы можете выбрать тип материала:
Общая информация
Похожие материалы
Рабочая программа по биологии 8 класс
Открытый урок «День земли»
Проект » Экология родного края»
Презентация «Методы биологических исследований. Значение биологии»
Самостоятельная работа “Средообразующая деятельность живого вещества. Круговорот веществ – основа целостности биосферы. Биосфера и здоровье человека”
Презентация «Влияние наркотиков на подростков»
Презентация «Бронхиальной астмы, как одно из острых состояний организма. Причины, симптомы, приступы, доврачебная помощь».
Самостоятельная работа “Пластиды и митохондрии. Рибосомы”
Не нашли то что искали?
Воспользуйтесь поиском по нашей базе из
5354775 материалов.
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Безлимитный доступ к занятиям с онлайн-репетиторами
Выгоднее, чем оплачивать каждое занятие отдельно
Минпросвещения сформирует новый федеральный перечень учебников
Время чтения: 2 минуты
Учителям предлагают 1,5 миллиона рублей за переезд в Златоуст
Время чтения: 1 минута
Путин поручил не считать выплаты за классное руководство в средней зарплате
Время чтения: 1 минута
ОНФ проверит качество охраны в российских школах
Время чтения: 2 минуты
В России предложили учредить День семейного волонтерства
Время чтения: 2 минуты
В Ленобласти педагоги призеров и победителей олимпиады получат денежные поощрения
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
О живой материи. Белки
Более 4 млрд лет назад на Земле из маленьких неорганических молекул непостижимым образом возникли белки, ставшие строительными блоками живых организмов. Своим бесконечным разнообразием всё живое обязано именно уникальным молекулам белка, и иные формы жизни во Вселенной науке пока неизвестны.
Белки, или протеины (от греч. «протос» — «первый»), — это природные органические соединения, которые обеспечивают все жизненные процессы любого организма. Из белков построены хрусталик глаза и паутина, панцирь черепахи и ядовитые вещества грибов. С помощью белков мы перевариваем пищу и боремся с болезнями. Благодаря особым белкам по ночам светятся светлячки, а в глубинах океана мерцают таинственным светом медузы.
Белковых молекул в живой клетке во много раз больше, чем всех других (кроме воды, разумеется!). Учёные выяснили, что у большинства организмов белки составляют более половины их сухой массы. И разнообразие видов белков очень велико — в одной клетке такого маленького организма, как бактерия Escherichia сой’ (см. дополнительный очерк «Объект исследования — прокариоты»), насчитывается около 3 тыс. различных белков.
БИОЛОГИЧЕСКИЕ «БУСЫ»
Молекула белка очень длинная. Химики называют такие молекулы полимерными (от греч. «поли» — «много» и «мерос» — «часть», «доля»). Действительно, длинная молекула полимера состоит из множества маленьких молекул, связанных друг с другом. Так нанизываются на нить бусинки в ожерелье. В полимерах роль нити играют химические связи между бусинками-молекулами.
Секрет белков спрятан в особенностях этих самых бусинок. Большинство полимеров не принимает устойчивой формы в пространстве, уподобляясь тем же бусам, у которых и не может быть пространственной структуры: повесишь их на шею — они примут форму кольца или овала, положишь в коробку — свернутся в клубок неопределённой формы. А теперь представим себе, что некоторые бусинки могут «слипаться» друг с другом. Например, красные притягиваются к жёлтым. Тогда вся цепочка примет определённую форму, обязанную своим существованием «слипа-нию» жёлтых и красных бусинок
Нечто подобное происходит и в белках. Отдельные маленькие молекулы, входящие в состав белка, обладают способностью «слипаться», так как между ними действуют силы притяжения. В результате у любой белковой цепи есть характерная только для неё пространственная структура. Именно она определяет чудесные свойства белков. Без такой структуры они не могли бы выполнять те функции, которые осуществляют в живой клетке.
При длительном кипячении белков в присутствии сильных кислот или щелочей белковые цепи распадаются на составляющие их молекулы, называемые аминокислотами. Аминокислоты — это и есть те «бусинки», из которых состоит белок, и устроены они сравнительно просто.
КАК УСТРОЕНА АМИНОКИСЛОТА
В природе встречаются также аминокислоты, в которых NH^-группа связана с более отдалёнными от карбоксильной группы атомами углерода. Однако для построения белков природа выбрала именно а-аминокислоты. Это обусловлено прежде всего тем, что только а-аминокислоты, соединённые в длинные цепи, способны обеспечить достаточную прочность и устойчивость структуры больших белковых молекул.
Число а-аминокислот, различающихся R-группой, велико. Но чаще других в белках встречается всего 20 разных аминокислот. Их можно рассматривать как алфавит «языка» белковой молекулы. Химики называют эти главные аминокислоты стандартными, основными или нормальными. Условно основные аминокислоты делят на четыре класса.
Для нормальной жизнедеятельности организм нуждается в полном наборе из 20 основных a-Z-аминокислот. Но одни из них могут быть синтезированы в клетках самого организма, а другие — должны поступать в готовом виде из пищевых продуктов. В первом случае аминокислоты называют заменимыми, а во втором — незаменимыми. Набор последних для разных организмов различен. Например, для белой крысы незаменимыми являются 10 аминокислот, а для молочнокислых бактерий — 16. Растения могут самостоятельно синтезировать самые разнообразные аминокислоты, создавать такие, которые не встречаются в белках.
ЧТО ТАКОЕ ПЕПТИД
Полимерная молекула белка образуется при соединении в длинную цепочку бусинок-аминокислот. Они нанизываются на нить химических связей благодаря имеющимся у всех аминокислот амино- и карбоксильной группам, присоединённым к а-атому углерода.
Образующиеся в результате такой реакции соединения называются пеп-тидами; (—СО— NH —группировка в них — это пептидная группа, а связь между атомами углерода и азота — пептидная связь (её ещё называют амидной). Соединяя аминокислоты посредством пептидных связей, можно получить пептиды, состоящие из остатков очень многих аминокислот. Такие соединения получили название полипептиды. Полипептидное строение белковой молекулы доказал в 1902 г. немецкий химик Эмиль Герман Фишер.
Общее число аминокислотных остатков в белковой молекуле изменяется в очень широких пределах. Так, человеческий инсулин состоит из 51 аминокислотного остатка, а лизо-цим молока кормящей матери — из 130. В гемоглобине человека 4 аминокислотные цепочки, каждая из которых построена из примерно 140 аминокислот. Существуют белки, имеющие почти 3 тыс. аминокислотных остатков в единой цепи.
Молекулярные массы белков лежат в диапазоне примерно от 11 тыс. для малых белков, состоящих из 100 аминокислотных остатков, до 1 млн и более для белков с очень длинными полипептидными цепями или для белков, состоящих из нескольких по-липептидных цепей.
Возникает вопрос: как же всё огромное многообразие белков с различными функциями и свойствами может быть создано всего из 20 молекул? А разгадка этого секрета природы проста — каждый белок имеет свой неповторимый аминокислотный состав и уникальный порядок соединения аминокислот, называемый первичной структурой белка.
СПИРАЛИ И СЛОИ
В начале 50-х гг. XX в. американские химики Лайнус Карл Полинг (1901— 1994), награждённый Нобелевской премией за исследования природы химической связи, и Роберт Кори (1897—1971) предположили, что некоторые участки аминокислотной цепочки в белках закручены в спираль. Благодаря совершенствованию экспериментальных методов (структуру белков изучают с помощью рентгеновских лучей) через несколько лет эта гениальная догадка подтвердилась.
Действительно, полипептидные цепи очень часто образуют спираль, закрученную в правую сторону. Это первый, самый низкий уровень пространственной организации белковых цепочек Здесь-то и начинают играть роль слабые взаимодействия «бусинок»-аминокислот: группа С=0 и группа N — H из разных пептидных связей могут образовывать между собой водородную связь. Оказалось, что в открытой Полингом и Кори спирали такая связь образована между группой С=0 каждой г-й аминокислоты и группой N — H ( i + 4)-й аминокислоты, т. е. между собой связаны аминокислотные остатки, отстоящие друг от друга на четыре «бусинки». Эти водородные связи и стабилизируют такую спираль в целом. Она получила название a.-спирали.
Позднее выснилось, что а-спираль — не единственный способ укладки аминокислотных цепочек. Помимо спиралей они образуют ещё и слои. Благодаря всё тем же водородным связям между группами С=0 и N — H друг с другом могут «слипаться» сразу несколько разных фрагментов одной полипептидной цепи. В результате получается целый слой — его назвали ^-слоем.
В большинстве белков а-спирали и р-слои перемежаются всевозможными изгибами и фрагментами цепи без какой-либо определённой структуры. Когда имеют дело с пространственной структурой отдельных участков белка, говорят о вторичной структуре белковой молекулы.
БЕЛОК В ПРОСТРАНСТВЕ
Для того чтобы получить полный «портрет» молекулы белка, знания первичной и вторичной структуры недостаточно. Эти сведения ещё не дают представления ни об объёме, ни о форме молекулы, ни тем более о расположении участков цепи по отношению друг к другу. А ведь все спирали и слои каким-то образом размещены в пространстве. Общая пространственная структура поли-пептидной цепи называется третичной структурой белка.
При образовании третичной структуры белка наконец-то проявляют активность R-группы — боковые цепи аминокислот. Именно благодаря им «слипаются» между собой большинство «бусинок»-аминокислот, придавая цепи определённую форму в пространстве.
В живом организме белки всегда находятся в водной среде. А самое большое число основных аминокислот — восемь — содержат неполярные R-группы. Разумеется, белок стремится надёжно спрятать внутрь своей молекулы неполярные боковые цепи, чтобы ограничить их контакт с водой. Учёные называют это возникновением гидрофобных взаимодействий (см. статью «Мельчайшая единица живого»).
Благодаря гидрофобным взаимодействиям вся полипептидная цепочка принимает определённую форму в пространстве, т. е. образует третичную структуру.
В молекуле белка действуют и другие силы. Часть боковых цепей основных аминокислот заряжена отрицательно, а часть — положительно. Так как отрицательные заряды притягиваются к положительным, соответствующие «бусинки» «слипаются». Электростатические взаимодействия, или, как их называют иначе, солевые мостики, — ещё одна важная сила, стабилизирующая третичную структуру.
У семи основных аминокислот есть полярные боковые цепи. Между ними могут возникать водородные связи, тоже играющие немалую роль в поддержании пространственной структуры белка.
Между двумя аминокислотными остатками цистеина иногда образуются ковалентные связи (— S —S—), которые очень прочно фиксируют расположение разных участков белковой цепи по отношению друг к другу. Такие связи называют дисуль-фидными мостиками. Это самые немногочисленные взаимодействия в белках (в некоторых случаях они вообще отсутствуют), зато по прочности они не имеют равных.
ВЫСШИЙ УРОВЕНЬ ПРОСТРАНСТВЕННОЙ ОРГАНИЗАЦИИ БЕЛКОВ
Молекула белка может состоять не из одной, а из нескольких полипептидных цепей. Каждая такая цепь представляет собой самостоятельную пространственную структуру — субъединицу. Например, белок гемоглобин состоит из четырёх субъединиц, которые образуют единую молекулу, располагаясь в вершинах почти правильного тетраэдра. Субъединицы «прилипают» друг к другу благодаря тем же самым силам, что стабилизируют третичную структуру. Это гидрофобные взаимодействия, солевые мостики и водородные связи.
Если белок состоит из нескольких субъединиц, говорят, что он обладает четвертичной структурой. Такая структура представляет собой высший уровень организации белковой молекулы. В отличие от первых трёх уровней четвертичная структура есть далеко не у всех белков. Приблизительно половина из известных на сегодняшний день белков её не имеют.
ПОЧЕМУ БЕЛКИ БОЯТСЯ ТЕПЛА
Связи, поддерживающие пространственную структуру белка, довольно легко разрушаются. Мы с детства знаем, что при варке яиц прозрачный яичный белок превращается в упругую белую массу, а молоко при скисании загустевает. Происходит это из-за разрушения пространственной структуры белков альбумина в яичном белке и казеина (огглат. caseus — «сыр») в молоке. Такой процесс называется денатурацией. В первом случае её вызывает нагревание, а во втором — значительное увеличение кислотности (в результате жизнедеятельности обитающих в молоке бактерий). При денатурации белок теряет способность выполнять присущие ему в организме функции (отсюда и название процесса: от лат. denaturare — «лишать природных свойств»). Денатурированные белки легче усваиваются организмом, поэтому одной из целей термической обработки пищевых продуктов является денатурация белков.
ЗАЧЕМ НУЖНА ПРОСТРАНСТВЕННАЯ СТРУКТУРА
В природе почти ничего не происходит случайно. Если белок принял определённую форму в пространстве, это должно служить достижению какой-то цели. Действительно, только белок с «правильной» пространственной структурой может обладать определёнными свойствами, т. е. выполнять те функции в организме, которые ему предписаны. А делает он это с помощью всё тех же R-групп аминокислот. Оказывается, боковые цепи не только поддерживают «правильную» форму молекулы белка в пространстве. R-группы могут связывать другие органические и неорганические молекулы, принимать участие в химических реакциях, выступая, например, в роли катализатора.
Часто сама пространственная организация полипептидной цепи как раз’ и нужна для того, чтобы сосредоточить в определённых точках пространства необходимый для выполнения той или иной функции набор боковых цепей. Пожалуй, ни один процесс в живом организме не проходит без участия белков.
В ЧЁМ СЕКРЕТ ФЕРМЕНТОВ
Все химические реакции, протекающие в клетке, происходят благодаря особому классу белков — ферментам. Это белки-катализаторы. У них есть свой секрет, который позволяет им работать гораздо эффективнее других катализаторов, ускоряя реакции в миллиарды раз.
Предположим, что несколько приятелей никак не могут встретиться. Но стоило одному из них пригласить друзей на день рождения, как результат не заставил себя ждать: все оказались в одном месте в назначенное время.
Чтобы встреча состоялась, понадобилось подтолкнуть друзей к контакту. То же самое делает и фермент. В его молекуле есть так называемые центры связывания. В них расположены привлекательные для определённого типа химических соединений (и только для них!) «уютные кресла» — R-группы, связывающие какие-то участки молекул реагирующих веществ. Например, если одна из молекул имеет неполярную группу, в центре связывания находятся гидрофобные боковые цепи. Если же в молекуле есть отрицательный заряд, его будет поджидать в молекуле фермента R-груп па с положительным зарядом.
В результате обе молекулы реагентов связываются с ферментом и оказываются в непосредственной близости друг от друга. Мало того, те их группы, которые должны вступить в химическую реакцию, сориентированы в пространстве нужным для реакции образом. Теперь за дело принимаются боковые цепи фермента, играющие роль катализаторов. В ферменте все «продумано» таким образом, что R-группы-катализаторы тоже расположены вблизи от места событий, которое называют активным центром. А после завершения реакции фермент «отпускает на волю» молекулы-продукты (см. статью «Ферменты — на все руки мастера»).
ОТКУДА БЕРЁТСЯ ИММУНИТЕТ
Белки выполняют в организме множество функций; они, например, защищают клетки от нежелательных вторжений, предохраняют их от повреждений. Специальные белки — антитела обладают способностью распознавать проникшие в клетки бактерии, вирусы, чужеродные полимерные молекулы и нейтрализовывать их.
У высших позвоночных от чужеродных частиц организм защищает иммунная система. Она устроена так, что организм, в который вторглись такие «агрессоры» — антигены, начинает вырабатывать антитела. Молекула антитела прочно связывается с антигеном: у антител, как и у ферментов, тоже есть центры связывания. Боковые цепи аминокислот расположены в центрах таким образом, что антиген, попавший в эту ловушку, уже не сможет вырваться из «железных лап» антитела. После связывания с антителом враг выдворяется за пределы организма.
Можно ввести в организм небольшое количество некоторых полимерных молекул, входящих в состав бактерий или вирусов-возбудителей какой-либо инфекционной болезни.
В организме немедленно появятся соответствующие антитела. Теперь попавший в кровь или лимфу «настоящий» болезнетворный микроб тотчас же подвергнется атаке этих антител, и болезнь будет побеждена. Такой способ борьбы с инфекцией есть не что иное, как нелюбимая многими прививка. Благодаря ей организм приобретает иммунитет к инфекционным болезням.
ДЛЯ ЧЕГО В ГЕМОГЛОБИНЕ ЖЕЛЕЗО
В природе существуют белки, в которых помимо аминокислот содержатся другие химические компоненты, такие, как липиды, сахара, ионы металлов. Обычно эти компоненты играют важную роль при выполнении белком его биологической функции. Так, перенос молекул и ионов из одного органа в другой осуществляют транспортные белки плазмы крови. Белок гемоглобин (от греч. «гема» — «кровь» и лат. globus — «шар», «шарик»), содержащийся в кровяных клетках — эритроцитах (от греч. «эритрос» — «красный» и «китос» — «клетка»), доставляет кислород от лёгких к тканям. В молекуле гемоглобина есть комплекс иона железа Fe 24 » со сложной органической молекулой, называемый гемам. Гемоглобин состоит из четырёх белковых субъединиц, и каждая из них содержит по одному гему.
В связывании кислорода в лёгких принимает участие непосредственно ион железа. Как только к нему хотя бы в одной из субъединиц присоединяется кислород, сам ион тут же чуть-чуть меняет своё расположение в молекуле белка. Движение железа «провоцирует» движение всей аминокислотной цепочки данной субъединицы, которая слегка трансформирует свою третичную структуру.
Другая субъединица, ещё не присоединившая кислород, «чувствует», что произошло с соседкой. Её структура тоже начинает меняться. В итоге вторая субъединица связывает кислород легче, чем первая. Присоединение кислорода к третьей и четвёртой субъединицам происходит с ещё меньшими трудностями. Как видно, субъединицы помогают друг другу в работе. Для этого-то гемоглобину и нужна четвертичная структура. Оксид углерода СО (в просторечии угарный газ) связывается с железом в геме в сотни раз прочнее кислорода. Угарный газ смертельно опасен для человека, поскольку лишает гемоглобин возможности присоединять кислород.
А ЕЩЁ БЕЛКИ.
. Служат питательными веществами. В семенах многих растений (пшеницы, кукурузы, риса и др.) содержатся пищевые белки. К ним относятся также альбумин — основной компонент яичного белка и казеин — главный белок молока. При переваривании в организме человека белковой пищи происходит гидролиз пептидных связей. Белки «разбираются» на отдельные аминокислоты, из которых организм в дальнейшем «строит» новые пептиды или использует для получения энергии. Отсюда и название:
греческое слово «пептос» означает «переваренный». Интересно, что гидролизом пептидной связи управляют тоже белки — ферменты.
. Участвуют в регуляции клеточной и физиологической активности. К подобным белкам относятся многие гормоны (от греч. «гормао» — «побуждаю»), такие, как инсулин, регулирующий обмен глюкозы, и гормон роста.
. Наделяют организм способностью изменять форму и передвигаться. За это отвечают белки актин и миозин, из которых построены мышцы.
. Выполняют опорную и защитную функции, скрепляя биологические структуры и придавая им прочность. Кожа представляет собой почти чистый белок коллаген, а волосы, ногти и перья состоят из прочного нерастворимого белка кератина.
ЧТО ЗАПИСАНО В ГЕНАХ
Последовательность аминокислот в белках кодируется генами, которые хранятся и передаются по наследству с помощью молекул ДНК (см. статьи «Хранитель наследственной информации. ДНК» и «Экспрессия генов»). Пространственную структуру белка задаёт именно порядок расположения аминокислот. Получается, что не только первичная, но и вторичная, третичная и четвертичная структуры белков составляют содержание наследственной информации. Следовательно, и выполняемые белками функции запрограммированы генетически. Громадный перечень этих функций позволяет белкам по праву называться главными молекулами жизни. Поэтому сведения о белках и есть то бесценное сокровище, которое передаётся в природе от поколения к поколению.
Интерес человека к этим органическим соединениям с каждым годом только увеличивается. Сегодня учёные уже расшифровали структуру многих белковых молекул. Они выясняют функции самых разных белков, пытаются определить взаимосвязь функций со структурой. Установление сходства и различий у белков, выполняющих аналогичные функции у разных живых организмов, позволяет глубже проникать в тайны эволюции.
АМИНОКИСЛОТЫ — ПОКАЗАТЕЛИ ВОЗРАСТА
ЗА ЧТО СЕНГЕР ПОЛУЧИЛ НОБЕЛЕВСКИЕ ПРЕМИИ
При гидролизе белков до аминокислот (разрушении пептидной связи водой) теряется информация о последовательности их соединения. Поэтому долгое время считали, что определение первичной структуры белка представляет собой совершенно безнадежную задачу. Но в 50-х гг. XX в. английский биохимик Фредерик Сенгер (родился в 1918 г.) смог расшифровать последовательность аминокислот в полипептидных цепях гормона инсулина. За эту работу, на выполнение которой ушло несколько лет, в 1958 г. Сенгер был удостоен Нобелевской премии по химии (двадцатью годами позже он совместно с У. Гилбертом получил вторую премию за вклад в установление первичной структуры ДНК).
Принципы определения аминокислотной последовательности, впервые сформулированные Сенгером, используются и ныне, правда, со всевозможными вариациями и усовершенствованиями. Процедура установления первичной структуры белка сложна и многоступенчата: в ней около десятка различных стадий. Сначала белок расщепляют до отдельных аминокислот и устанавливают их тип и количество в данном веществе. На следующей стадии длинную белковую молекулу расщепляют уже не полностью, а на фрагменты. Затем в этих фрагментах определяют порядок соединения аминокислот, последовательно отделяя их одну за другой. Расшепление белка на фрагменты проводят несколькими способами, чтобы в разных фрагментах были перекрывающиеся участки. Выяснив порядок расположения аминокислот во всех фрагментах, получают полную информацию о том, как аминокислоты расположены в белке. К концу XX в. созданы специальные приборы, определяющие последовательность аминокислот в молекуле белка в автоматическом режиме — секвенаторы (от англ. sequence — «последовательность»).
МОЛОКО И КИСЛОМОЛОЧНЫЕ ПРОДУКТЫ
Молоко представляет собой коллоидный раствор жира в воде. Под микроскопом хорошо видно, что оно неоднородно: в бесцветном растворе (сыворотке) плавают жировые шарики.
Входящий в состав молока сахар лактоза С^НддО,, изомерен сахарозе. В организме человека под действием фермента лактазы этот сахар расщепляется на моносахариды глюкозу и галактозу, которые легко усваиваются. За счёт этого, например, грудные дети пополняют запасы углеводов. Интересно, что у многих людей (в основном у представителей монголоидной расы) организм в зрелом возрасте утрачивает способность расщеплять лактозу.
Проходя через пищеварительный тракт, лактоза не усваивается, а становится питательной средой для развития различных болезнетворных микроорганизмов, что приводит к общему недомоганию. Именно поэтому народы Дальнего Востока (японцы, китайцы) практически не употребляют в пишу молочные продукты.
с„н„о„ + н,о =лактоза == 4СНзСН(ОН)СООН. молочная (2-гидроксипропановая) кислота
Именно молочная кислота определяет специфический вкус кефира. По мере того как она накапливается в растворе, происходит коагуляция (свёртывание)казеина, который выделяется в свободном виде. Поэтому кефир имеет более густую консистенцию, чем молоко. Молочнокислое сбраживание лактозы сопровождается спиртовым брожением, из-за чего в кисломолочных продуктах, в частности в кефире, есть небольшое количество алкоголя (до 0,03 %). В кисломолочных продуктах содержатся также микроорганизмы, которые подавляют развитие болезнетворных бактерий и тем самым улучшают пишеварение.
Творог тоже получают сквашиванием молока молочнокислыми бактериями. Его главной составной частью является белок казеин.
МЕДНАЯ КРОВЬ
Кроме кальмаров, кислород переносится “голубой кровью” также у десятиногих ракообразных (омары, крабы, креветки). Гемоиианин найден у всех головоногих моллюсков (осьминоги, кальмары, каракатицы), разнообразных улиток, пауков и др. А вот у морских гребешков, устриц и других двустворчатых моллюсков его нет.
Из гемоиианина нетрудно полностью извлечь медь. Аля этого достаточно обработать белок в отсутствие кислорода реактивом, который прочно связывается с ионами одновалентной меди. Таким же способом можно определить содержание меди в гемоиианине. Лишённый этого металла, он теряет способность переносить кислород. Но если потом ввести в раствор белка ионы Си»1′, гемоиианин восстанавливает свою физиологическую активность.
Так было доказано, что в отсутствие кислорода медь гемоиианина находится в степени окисления +1. При избытке же этого газа происходит частичное окисление металла. При этом всегда на одну связанную гемоиианином молекулу кислорода приходится два атома меди. Таким образом, кислород окисляет ровно половину атомов меди. Это ещё одно отличие гемоиианина от значительно более распространённого в животном мире гемоглобина, в котором все атомы железа равноценны и имеют заряд +2 как в свободном состоянии, так и в комплексе с кислородом.